题目内容
【题目】小聪想到家里新换的水龙头。从说明书上了解到该水龙头是铜质镀铬。好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀请你一同参加。
(知识回放)
金属活动性顺序:K Ca Na MgAl Zn Fe Sn Pb (H) Cu_____Ag Pt Au。请你在横线上填写对应金属的元素符号。
(作出猜想)
猜想1.Cr>Fe>Cu; 猜想2. Fe>Cu >Cr; 猜想3.你的猜想是__________。
(查阅资料)
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密氧化膜。
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
(设计与实验)
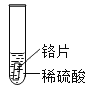
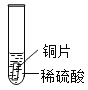
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸。
实验 | 试管1 | 试管2 | 试管3 |
实验 操作 |
|
|
|
实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | ________ |
(结论与解释)
(1)小聪得到的结论是猜想__________正确。
(2)实验前用砂纸打磨金属片的目的是_______________。
(知识运用)将铬片投入FeSO4溶液中,反应__________(填“能”或“不能”)进行。若能进行,请你写出反应的化学方程式____________。
【答案】Hg Fe>Cr>Cu 无明显现象 1 除去金属表面的氧化膜,利于反应的进行 能 Cr+FeSO4═Fe+CrSO4
【解析】
[知识回放]金属活动性顺序为K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au,故填:Hg;
[作出猜想]这三种金属的活动性顺序还可能是Fe>Cr>Cu,故填:Fe>Cr>Cu;
[设计与实验]铜在氢的后面,不会与稀硫酸反应,故表面没有明显的现象,故填:无明显现象;
[结论与解释](1)根据现象,铬片表面产生气泡较快,铁片表面产生气泡较慢,铜无明显现象发生,故这三种金属的活动性顺序为Cr>Fe>Cu,故猜想1正确,故填:1;
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应的进行,故填:除去金属表面的氧化膜,利于反应的进行;
[知识运用]铬的活动性比铁强,故各能与硫酸亚铁反应,反应生成硫酸铬和铁,故填:能,Cr+FeSO4═Fe+CrSO4。

 名题训练系列答案
名题训练系列答案 期末集结号系列答案
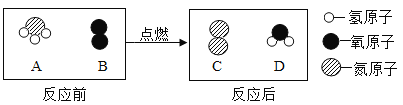
期末集结号系列答案【题目】我们知道,空气中氧气约占总体积的1/5,物质燃烧与空气中氧气密切相关。为此,小华进行了相关实验探究:
(实验探究)小华利用下列装置进行实验:

(实验操作及记录)(请你补充完整实验二)
实验 | 操作 | 现象 |
实验一 | 点燃酒精灯 | 硫燃烧,发出微弱的淡蓝色火焰 |
实验二 | 1.更换燃烧管(装有等量硫粉),挤压滴管A当观察到_____的现象时,可认为空气已经排尽 2.点燃酒精灯 | 硫没有燃烧 |
实验三 | 1.更换燃烧管(装有等量硫粉),挤压滴管B 2.当E处能使带火星的木条复燃时点燃酒精灯 | 硫燃烧很旺,发出明亮的蓝紫色火焰 |
(结果分析)
(1)对照实验一和实验_____的现象,说明硫燃烧需要氧气。
(2)对照实验三和实验一的现象,可知燃烧的剧烈程度与_____有关。
(交流与反思)小华为了进一步探究“是否只有纯氧才能使带火星的木条复燃”,又进行了以下实验:利用如图装置收集4瓶气体(集气瓶预先装满水,量筒规格为100mL),以带火星的木条进行检验。结果如下:
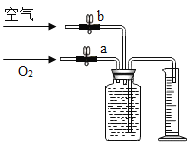
1号瓶 | 2号瓶 | 3号瓶 | 4号瓶 |
34mL O2+66mL 空气 | 35mL O2+65mL 空气 | 36mL O2+64mL 空气 | 37mL O2+63mL 空气 |
不复燃 | 不复燃,但很亮 | 很亮,复燃 | 立即复燃 |
据此可知,当O2的体积分数达到_____时(精确到1%),即可使带火星的小木条复燃。
(拓展资料)提供资料:
1.相同条件下,两种气体的体积比等于分子个数比。
2.硝酸铜固体加热分解生成氧化铜、二氧化氮和氧气。小华利用如图实验加热硝酸铜,发现收集的气体能使带火星木条复燃。请你根据该反应的化学方程式分析判断NO2_____(填“有”“无”或“无法确定”)助燃性。
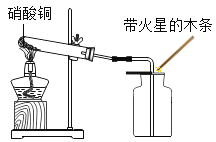
【题目】天然气作为清洁能源已成为我国现代化城市的首选燃料,LNG船是低温运输天然气的专用船舶,被喻为世界造船“皇冠上的明珠”。某兴趣小组的同学围绕着船舶使用的金属材料进行了研究。
(1)在焊接不锈钢管道时,通常要使用氩气作保护气,这是因为氩气的化学性质_________。
(2)金属在海水中易生锈腐蚀(铁生锈会得到红棕色的固体)。造船工业为了避免轮船的钢铁外壳被腐蚀,通常在轮船外壳镶嵌另外一种金属。利用该金属与铁的活动性的不同,保护铁不易被腐蚀。
(研究课题1)一般情况下,两种活动性不同的金属在潮湿的环境中接触时,哪种金属先被腐蚀呢?
(实验设计1)将打磨后的金属片进行如图所示的实验,
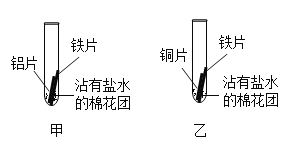
放置一段时间后将观察到的现象及分析填入下表:
现象 | 分析 |
甲中:铝片表面出现灰白色物质,铁片表面几乎没有明显现象。 | 铝与铁在潮湿的环境中接触,铝首先被腐蚀。 |
乙中:铁片表面出现___________,铜片表面几乎没有明显现象。 | 铁与铜在潮湿的环境中接触,铁首先被腐蚀。 |
(得出结论)一般情况下,两种活动性不同的金属在潮湿的环境中接触时,活动性较___________(填“强”或“弱”)的金属首先被腐蚀。
(知识应用)造船工业为避免轮船的钢铁外壳被腐蚀,通常在轮船外壳镶嵌的金属是_____(填编号)
A 银块 B 铜块 C 锡块 D 锌块
(3)LNG船还使用了大量的锌铜合金。
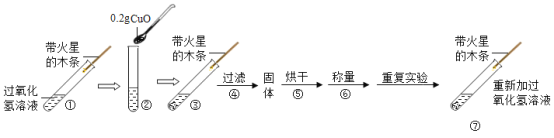
(研究课题2)测定锌铜合金中锌、铜的质量分数
(实验设计2)进行如图所示的实验。
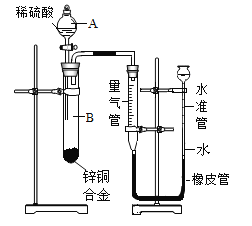
①图中量气管和水准管可用来测量气体体积,为准确测量氢气的体积,在读取量气管中液面读数的过程中,应注意________(填字母)。
A 读数时视线与凹液面最低处相平
B 读数前应上下移动水准管,待两管液面相平再读数
C 保持水准管静止,待水准管中液面不再上升时再读数
②实验前,将已经打磨过的块状锌铜合金加工成碎屑,其目的是:________。
③实验操作步骤:检查气密性,将药品和水装入各仪器中,连接好装置后,再次检查装置的气密性,记录量气管的液面位置为5mL,由A向B滴加足量试剂,待B中不再有气体产生并恢复至室温后,记录量气管的液面位置为85mL;将B中剩余固体过滤,洗涤,干燥,用电子天平称其质量为0.416克。
(数据处理)该实验条件下,氢气的密度是0.09gL-1。根据上述的数据计算锌铜合金中铜的质量分数_______。(请写出计算过程)
(误差分析)如果操作规范,计算正确,但通过本方案测出的铜的质量分数计算值总是低于真实值,其主要原因是:____________。