题目内容
【题目】如图是碘元素的部分信息及碘原子的结构示意图,下列说法正确的是 ( )

A.碘的相对原子质量为126.9g,原子核内质子数为53
B.碘原子核外共有53个电子,碘在周期表中位于第七周期
C.根据碘的原子结构示意图可推测碘元素与氯元素的化学性质相似
D.碘元素属于非金属元素,碘原子在化学反应中容易失去电子
【答案】C
【解析】
A、由图可知,碘的相对原子质量为126.9,原子结构示意图中,圆圈内的数字为53,即原子核内质子数为53,故不符合题意;
B、根据原子中,核内质子数等于核外电子数可得,碘原子核外共有53个电子,原子结构示意图中,碘原子核外有5个电子层,因此碘在周期表中位于第五周期,故不符合题意;
C、根据最外层电子数相同,化学性质相似的原则可得,碘原子与原子的最外层电子数都是7,化学性质相似的,故符合题意;
D、碘是“石”字旁,碘元素属于非金属元素,由原子结构示意图可知,碘原子的最外层电子数是7,大于4,在化学反应中容易得到电子,故不符合题意。

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案【题目】(1)请填写下列表格
化学符号 | __________ | 5CH4 | ____________ | P2O5 |
表示的意义 | 硫离子 | ___________ | “五粮液”主要成分 | 数字2的意义: ______________ |
(2)我国科学家张青莲教授主持测定的钢等多种元素的相对原子质量已成为国际标准。根据图1、图2完成下列内容。
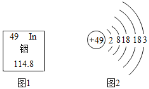
①铟属于______(填“金属”或“非金属”)元素,其相对原子质量为_______.
②铟的化学性质与铝的化学性质相似,原因是_______。铟元素在元素周期表中位于第___________周期。
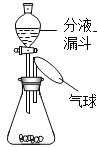
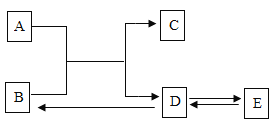
(3)铟与氯气(Cl2)反应生成氯化铟的微观过程可表示为:
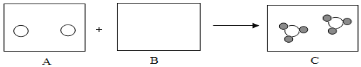
请将B框中的信息补充完整,你这样补充的理由是___________________________。
【题目】天然气作为清洁能源已成为我国现代化城市的首选燃料,LNG船是低温运输天然气的专用船舶,被喻为世界造船“皇冠上的明珠”。某兴趣小组的同学围绕着船舶使用的金属材料进行了研究。
(1)在焊接不锈钢管道时,通常要使用氩气作保护气,这是因为氩气的化学性质_________。
(2)金属在海水中易生锈腐蚀(铁生锈会得到红棕色的固体)。造船工业为了避免轮船的钢铁外壳被腐蚀,通常在轮船外壳镶嵌另外一种金属。利用该金属与铁的活动性的不同,保护铁不易被腐蚀。
(研究课题1)一般情况下,两种活动性不同的金属在潮湿的环境中接触时,哪种金属先被腐蚀呢?
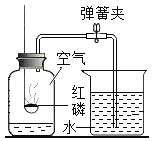
(实验设计1)将打磨后的金属片进行如图所示的实验,
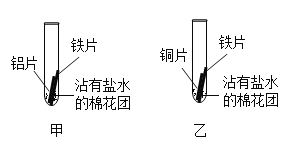
放置一段时间后将观察到的现象及分析填入下表:
现象 | 分析 |
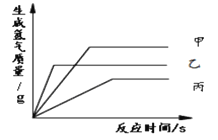
甲中:铝片表面出现灰白色物质,铁片表面几乎没有明显现象。 | 铝与铁在潮湿的环境中接触,铝首先被腐蚀。 |
乙中:铁片表面出现___________,铜片表面几乎没有明显现象。 | 铁与铜在潮湿的环境中接触,铁首先被腐蚀。 |
(得出结论)一般情况下,两种活动性不同的金属在潮湿的环境中接触时,活动性较___________(填“强”或“弱”)的金属首先被腐蚀。
(知识应用)造船工业为避免轮船的钢铁外壳被腐蚀,通常在轮船外壳镶嵌的金属是_____(填编号)
A 银块 B 铜块 C 锡块 D 锌块
(3)LNG船还使用了大量的锌铜合金。
(研究课题2)测定锌铜合金中锌、铜的质量分数
(实验设计2)进行如图所示的实验。
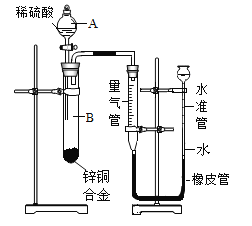
①图中量气管和水准管可用来测量气体体积,为准确测量氢气的体积,在读取量气管中液面读数的过程中,应注意________(填字母)。
A 读数时视线与凹液面最低处相平
B 读数前应上下移动水准管,待两管液面相平再读数
C 保持水准管静止,待水准管中液面不再上升时再读数
②实验前,将已经打磨过的块状锌铜合金加工成碎屑,其目的是:________。
③实验操作步骤:检查气密性,将药品和水装入各仪器中,连接好装置后,再次检查装置的气密性,记录量气管的液面位置为5mL,由A向B滴加足量试剂,待B中不再有气体产生并恢复至室温后,记录量气管的液面位置为85mL;将B中剩余固体过滤,洗涤,干燥,用电子天平称其质量为0.416克。
(数据处理)该实验条件下,氢气的密度是0.09gL-1。根据上述的数据计算锌铜合金中铜的质量分数_______。(请写出计算过程)
(误差分析)如果操作规范,计算正确,但通过本方案测出的铜的质量分数计算值总是低于真实值,其主要原因是:____________。
【题目】在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水。某课外兴趣小组对生成物中碳的氧化物种类等问题进行了如下探究:
(提示)①CO2+2NaOH=Na2CO3+H2O;②NaOH易溶于水;③浓硫酸能吸水;④氧化铁为红色粉末,铁粉为黑色固体。
(提出问题)生成物中有哪几种碳的氧化物?
猜想1 | 猜想2 | 猜想3 |
只有CO | 只有CO2 | ______ |
(设计实验)兴趣小组同学设计了如下实验:
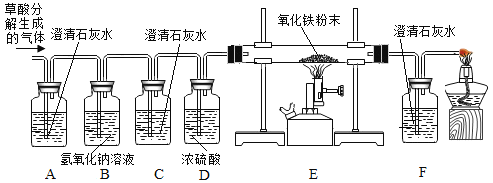
(实验探究)
(1)观察到_____装置(填字母)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成。该装置中发生反应的化学方程式为____________。C装置中作用是________
(2)观察到:①C装置中_________________ ,F装置中_____________;
②E装置中出现________的现象。
上述现象都能分别证明草酸分解的气体中含有CO。其中E装置中发生反应的化学方程式为_________。
(实验结论)猜测3成立。
(拓展与反思)
(1)装置末端酒精灯的作用是____;
(2)若B装置没有把二氧化碳气体完全吸收,可能的一条原因是_______;