题目内容
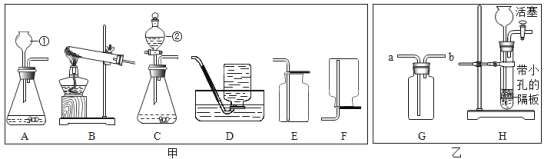
【题目】下图是实验室制取气体可能用到的装置。
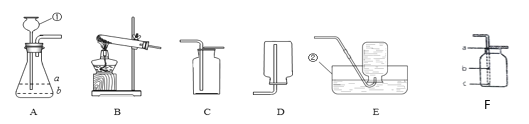
(1)写出编号仪器的名称:①_____,②______。
(2)实验室选用A装置制取CO2,加入药品前应先____,锥形瓶内的管口应插入到___(填“a”或“b”)处。若用B装置制取O2的化学方程式是____。
(3)利用装置F收集氧气,导管应伸到__(填“a”或“b”或“c”),验满二氧化碳的方法是将____放在导管___,(填“a”或“b”或“c”)熄灭则满。
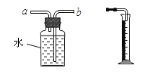
(4)若利用如图装置测量产生CO2的体积,应在水面上加上一层植物油,据此猜测CO2具有的一点性质是___,放入量筒中的导管应该和___端(填“a”或“b”)相连。若仰视读数为40ml,则收集到的气体体积____40ml(填“大于”或“小于”)。
(5)如果用KMnO4加热制取O2时,若收集到的气体不纯,可能的原因是______。演示铁丝在氧气中燃烧实验时,收集氧气时最好选用的装置是____(填装置序号),化学方程式为_______。
【答案】长颈漏斗 水槽 检查装置气密性 a 2KClO3 ![]() 2KCl+3O2↑ c 燃着的木条 a CO2能溶于水 b 大于 未等气泡连续均匀放出时就收集;向上排空法收集时导管没有伸到集气瓶底部;排水法收集时集气瓶内没有装满水或留有气泡(合理答案都可) E 3Fe+2O2
2KCl+3O2↑ c 燃着的木条 a CO2能溶于水 b 大于 未等气泡连续均匀放出时就收集;向上排空法收集时导管没有伸到集气瓶底部;排水法收集时集气瓶内没有装满水或留有气泡(合理答案都可) E 3Fe+2O2![]() Fe3O4
Fe3O4
【解析】
(1)仪器①的名称是长颈漏斗,故填长颈漏斗;
仪器②名称是水槽,故填水槽。
(2)制取气体时,在加入药品之前应检查装置的气密性,防止生成的气体逸散到空气中,故填检查装置的气密性;
固液常温发生装置中的长颈漏斗的管口应插到液面以下,防止生成的气体逸散到空气中,故填a;
图中试管口处没有棉花,用B装置制取O2的反应是氯酸钾在二氧化锰作催化剂和加热的条件下反应生成了氯化钾和氧气,故反应的化学方程式写为:2KClO3 ![]() 2KCl+3O2↑。
2KCl+3O2↑。
(3)利用向上排空气法收集氧气时,应将导管口伸到集气瓶的底部,以尽可能得排尽瓶内的空气,提高氧气的纯度,故填c;
验满二氧化碳的方法是将燃着的木条伸到集气瓶口处,木条熄灭,表明二氧化碳已经集满,故填燃着的木条;
验满二氧化碳的方法是将燃着的木条伸到集气瓶口处,故填a。
(4)植物油隔绝了二氧化碳与水接触,说明二氧化碳能溶于水,故填CO2能溶于水;
水的密度大于二氧化碳的密度,水要从长管流出,故填b;
读取量筒内液体体积数时,仰视读取,则液体的实际体积数大于读数,故填大于。
(5)用KMnO4加热制取O2收集到的气体不纯,可能的原因有未等气泡连续均匀放出时就收集;向上排空法收集时导管没有伸到集气瓶底部;排水法收集时集气瓶内没有装满水或留有气泡等,故填未等气泡连续均匀放出时就收集;向上排空法收集时导管没有伸到集气瓶底部;排水法收集时集气瓶内没有装满水或留有气泡(合理答案都可);
做铁丝在氧气中燃烧实验时,收集氧气时最好选用排水法,以便于集气瓶内留少量水,且排水法收集的气体也比较纯净,故填E;
铁丝和氧气在点燃的条件下反应生成四氧化三铁,故反应的化学方程式写为:3Fe+2O2![]() Fe3O4。
Fe3O4。

 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案【题目】某化学研究小组对当地的石灰石样品进行研究。称取石灰石样品8g,把50g稀盐酸分五次加入样品中,测得实验数据见下表(假设石灰石样品中的杂质不溶于水、不与盐酸反应,二氧化碳不溶解,氯化钙易溶于水)。
实验序号 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
第1次 | 10 | 6 |
第2次 | 10 | 4 |
第3次 | 10 | 2 |
第4次 | 10 | 1 |
第5次 | 10 | m |
请回答:(1)第5次剩余固体的质量m=__________g;
(2)石灰石样品中CaCO3的质量分数为多少_________?(写出计算过程,下同)
(3)反应结束后生成CO2的质量是多少_________?
【题目】实验创新是中学生最为重要的科学素养,以下是化学兴趣小组的同学在学习“二氧化锰催化过氧化氢分解制氧气实验”后,对实验的创新设计。
(实验一):设计新的实验装置
实验过程如下:
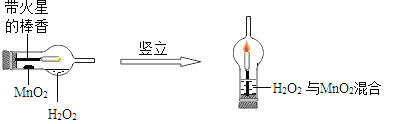
①将一支球形干燥管水平放置,用滴管吸取3ml(密度为1g/ml)质量分数为5%的H2O2加入干燥管的球泡中,再用药匙取0.2gMnO2粉末,加在干燥的进气管的管壁上;②点燃橡胶塞上固定的棒香后,塞紧干燥管并将其竖立,观察现象;
(1)可观察到带火星的棒香立即__________;
(2)下列各项是同学们对该创新实验的评价,你认为评价不合理的是 __________(填序号)
A.实验所用的仪器、材料及药品均易得到
B.实验室用的药品用量太大
C.反应速度太慢,耽误时间
D.实验现象明显,整个装置好似点燃的灯塔,趣味性强
(实验二):寻找新的催化剂
(实验探究)
实验步骤 | 实验现象 |
I. 分别量取5mL 5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象。 | A试管中产生气泡,带火星木条复燃。B试管中无明显现象。 |
II.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃。 |
III.将试验II中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥,称量。 | 所得的固体质量为_________________ |
IV.分别量取5mL5%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 |
(实验结论)
(1)A中产生的气体是_________;
(2)实验II可以证明:____________,再结合实验I和III的结论可以证明氧化铁可以作为过氧化氢分解的催化剂。
(3)写出氧化铁(Fe2O3)催化过氧化氢分解的文字表达式:______;
(实验评价)
(1)设计实验IV的目的是__________;
(2)若实验IV观察到D试管中产生气泡的速率更快,由此你可以得到的结论是_________。
(实验拓展)
查阅资料得知:CuO、CuSO4、猪肝、马铃薯等也可做过氧化氢溶液分解的催化剂,下列有关催化剂的说法正确的是________________
A.MnO2只能作为过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂能使原本不发生的反应也能快速进行
D.用作催化剂的物质不可能是其它反应的反应物或生成物