题目内容
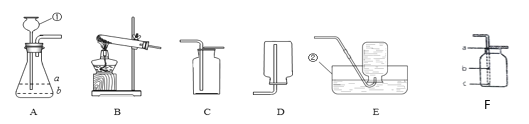
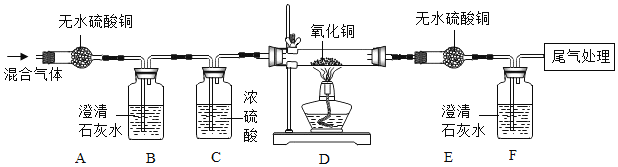
【题目】下图是实验室制取气体用到的部分装置,请按照要求回答:
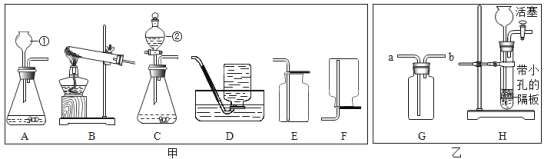
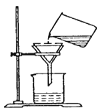
(1)仪器②的名称___________.
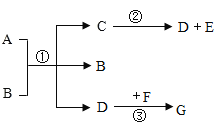
(2)某同学用加热高锰酸钾的方法制备氧气,他应选用的气体发生装置是_______(在图甲中选择,填序号),发生反应的化学方程式为___________________.
(3)因为氧气具有________________的性质,所以可以选用装置D来收集氧气;又因为氧气密度比空气略大,所以可以选用装置________(在图甲中选择,填序号)进行收集.
(4)有同学用A和D装置制取氧气,但最终只收集到了少量氧气。产生这种结果的最主要原因是__________________________。
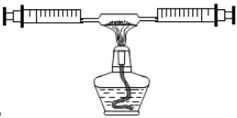
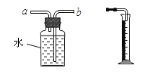
(5)老师提醒可以用图乙中的装置进行氢气的制取。用H装置制氢气的最大优点是______;装置H的气密性检查方法是,先加水形成液封并关闭活塞,然后__________,若________,则装置气密性良好。若用G装置收集氢气,则应将发生装置的导管与装置G的导管____(选填“a”或“b”)相连接。
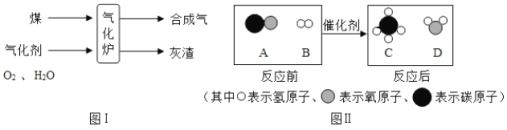
【答案】分液漏斗 B 2KMnO4![]() K2MnO4+MnO2+O2↑ 不易溶于水 E 长颈漏斗下端管口没有伸到液面以下 可以控制反应的发生和停止 继续加水 漏斗中有一段稳定的水注 b
K2MnO4+MnO2+O2↑ 不易溶于水 E 长颈漏斗下端管口没有伸到液面以下 可以控制反应的发生和停止 继续加水 漏斗中有一段稳定的水注 b
【解析】
(1)据图可知仪器②的名称是分液漏斗;
(2)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,所以应选择的发生装置是B;高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)氧气不易溶于水,可用排水法收集;氧气的密度比空气的密度大,因此能用向上排空气法收集;
(4)长颈漏斗下端管口没有伸到液面以下,造成生成的气体从长颈漏斗中逸出;
(5)H装置中的有空塑料板上放锌粒,反应发生时打开开关,硫酸从长颈漏斗内流下,与锌粒接触反应开始,当关闭开关时气体无法排出,压强越来大,把硫酸又压回到长颈漏斗内,使锌粒与硫酸分离,所以反应停止,所以该装置可以控制反应的发生和停止;装置H的气密性检查方法是,先加水形成液封并关闭活塞,然后继续加水,若漏斗中有一段稳定的水注,则装置气密性良好;若用G装置采用排空法收集氢气,氢气的密度小于空气的密度,氢气应从“短进长出”。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案