题目内容
【题目】小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬.好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,请把以下探究过程补充完全.
(作出猜想):1.Cr>Fe>Cu 2. Fe>Cu>Cr 3.________.
(查阅资料)(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
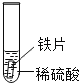
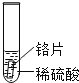
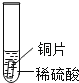
(设计与实验)小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种浓度的稀硫酸.
实验 | 试管1 | 试管2 | 试管3 |
实验操作 |
|
|
|
实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变为蓝色 | 无明显现象 |
(结论与解释)(1)小聪得到的结论是猜想________ 正确.
(2)实验前用砂纸打磨金属片的目的是________.
(知识运用)如果将光洁的铬片投入到CuSO4溶液中,反应的现象为______.反应的化学方程式为_______.
【答案】Fe>Cr>Cu 1 除去金属表面的氧化膜 铬片表面有红色固体生成 Cr+CuSO4=Cu+CrSO4
【解析】
[作出猜想]根据金属活动性顺序可知,铁的金属活动性一定在铜的前面,三种金属的活动性顺序可能存在三种情况:猜想1为Cr>Fe>Cu;猜想2为Fe>Cu>Cr,故猜想3为:Fe>Cr>Cu;
故填:Fe>Cr>Cu;
[结论与解释](1)试管1中实验现象铁片表面产生气泡较慢,溶液变为浅绿色,可知金属铁在金属活动顺序中排在氢前,根据铬片表面产生气泡较快,溶液变为蓝色,从而得出铬也排在氢前且铬比铁活泼,因为铜不能和稀硫酸反应生成氢气,可知铜排在氢的后面,故猜想1.Cr>Fe>Cu正确;
故填:1;
(2)因为金属的表面常有一层金属氧化物会影响金属和酸溶液的反应,因此实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应;
故填:除去金属表面的氧化膜;
[知识运用]有上述实验可知,铬的活动性比铜强,故铬能和硫酸铜反应生成硫酸铬和铜,则反应的化学方程式为:Cr+CuSO4=Cu+CrSO4;
故填:Cr+CuSO4=Cu+CrSO4。