题目内容
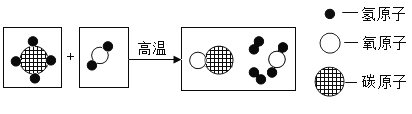
【题目】下图是氯、钙元素在元素周期表中的信息,C是一种原子的结构示意图。
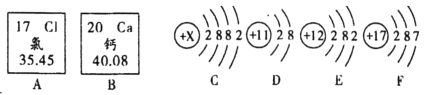
(1)图C中X数值是__________; D、E、F中与C中元素化学性质相似的是_________(填序号)。
(2)写出图B中元素形成离子的符号_____________;D、E、F中表示离子的是________②(填序号)。
(3)F中元素与地壳中含量最多的金属元素形成的化合物的化学式为__________;A与B两种元素的本质区别是_____________。
【答案】20 E Ca2+ D AlCl3 质子数不同
【解析】
在原子中,质子数=核外电子数,最外层电子数决定元素化学性质。
(1)在原子中,质子数=核外电子数,故![]() ,元素化学性质取决于最外层电子数,D、E、F中与C元素最外层电子数相同的是E,故选E。
,元素化学性质取决于最外层电子数,D、E、F中与C元素最外层电子数相同的是E,故选E。
(2)Ca最外层电子数为2,容易失去电子,故离子符号为Ca2+,电子数与质子数不相等时表示为离子,故选D。
(3)F是氯元素,地壳中最多的金属元素为Al,与Cl元素组合得AlCl3,质子数不相等为元素种类不同的原因,故A与B两种元素的本质区别是质子数不同。

练习册系列答案
相关题目
【题目】请从 A 或B 两题中任选一个作答,若两题均作答,按 A 计分。
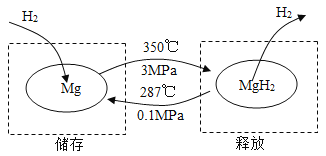
在一定条件下,Mg 和 MgH2的相互转化可以实现氢气的储存和释放。其工作原理如图。
A | B |
(1)氢气储存时发生反应的化学方程式为_______。 (2)氢气很容易逃逸,若氢气存储效率为 10%,储存 1 kg 氢气,至少需要 Mg 的质量为_______ kg。 | (1)氢气释放时发生反应的化学方程式 为_______。 (2)理论上,52 kg MgH2最多能释放氢气的质量为_______ kg。 |