题目内容
【题目】溶解度是我们初中化学常见的概念,请回答下列问题。
I.下表是NaC1、KNO3在不同温度下的溶解度:
温度/℃ | 0 | 20 | 40 | 60 | 80 | |
溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | |
(1)要比较NaC1、KNO3在水中的溶解能力,需要控制的变量是水的质量和_____________________。
(2)从KNO3溶液中获取其晶体适宜的方法是_____________________。
(3)20℃时,各取NaC1、KNO3固体3.5g加入10g水中,充分溶解后达到饱和状态的是___溶液。
(4)若将上述数据在坐标中绘制成NaCl、KNO3的溶解度曲线,两条曲线的交,点对应的温度范围是(_____)
A 0°C~20°C
B 20°C ~40°C
C 40°C ~60°C
D 60°C ~80°C
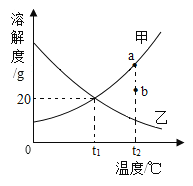
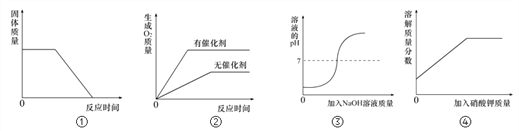
II.将质量为30g的B物质加入到50g水中,充分搅拌后,剩余物质的质量随温度的关系如图所示,过程中不考虑水分蒸发,回答问题:
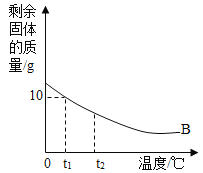
(5)固体B的溶解度随温度的升高而____________(填“增大”或“减小”) 。
(6) t1℃时,B的溶解度是___________。
【答案】温度 降温结晶 KNO3 B 增大 40g
【解析】
(1)若要比较KNO3与 NaCl在水中的溶解能力,需要控制的变量是水的质量和温度;故填:温度;
(2)由表格数据可知,硝酸钾的溶解度受温度影响比较大,所以可采用降温结晶的方法获取硝酸钾晶体;故填:降温结晶;
(3)20℃时NaCl、KNO3固体的溶解度分别为36.0g、31.6g,则该温度下,10g水中分别溶解3.6g氯化钠或3.16g硝酸钾就能达到饱和状态;20℃时,各取NaCl、KNO3固体3.5g分别加入10g水中,充分溶解后达到饱和状态的是硝酸钾溶液;故填:KNO3;
(4)由表中的硝酸钾和氯化钠不同温度下的溶解度数据可知:若两物质的溶解度相等,此时所对应的温度范围在20℃~40℃.故填:B;
(5)由图可知,随着温度的升高剩余固体在不断减少,说明随温度的升高,固体B的溶解度在增大;故填:增大;
(6)由图可知,t1℃时,50g水中最多溶解了20gB物质,则该温度下,100g水中最多可溶解40gB物质,B的溶解度是40g;故填:40g。

 寒假学与练系列答案
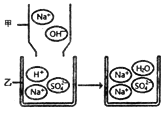
寒假学与练系列答案【题目】实验室有一瓶标签破损的硫酸。为测定该瓶硫酸溶液的溶质质量分数,小强同学在烧杯中加入50g该硫酸,然后向烧杯中滴加溶质质量分数为10%的氢氧化钠溶液,边滴加边搅拌,随着氢氧化钠溶液的滴入,溶液的pH变化情况如下表所示,请分析并计算:
氢氧化钠溶液的质量/g | 溶液的pH | 所得溶液 |
30 | pH<7 | a |
40 | pH =7 | b |
45 | pH>7 | c |
(1)a、b、c三种溶液中只含一种溶质的是________。
(2)该瓶硫酸溶液的溶质质量分数是多少____?(写出解题过程)(H2SO4+2NaOH==Na2SO4+2H2O)