题目内容
【题目】(7分)水和溶液在生产、生活中起着十分重要的作用。
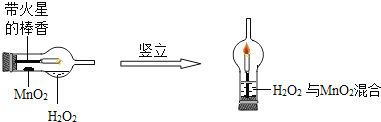
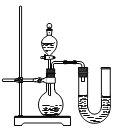
(1)下图是电解水实验装置。在实验过程中,试管1产生的气体是 ,写出水在通电条件下反应的化学方程式 。
(2)将源水处理成自来水的过程中需加入生石灰,生石灰与水反应的化学方程式为__ __。
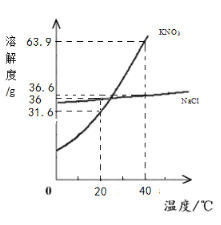
(3)20℃时,氯化钠的溶解度为36g,则20℃时氯化钠饱和溶液中溶质和溶剂的质量比为 。
(4)为了进行农业选种,现将200g30%的氯化钠溶液稀释为10%的氯化钠溶液,需要加水的质量为 。
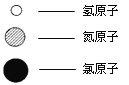
(5)自来水中通入少量氯气可以杀菌消毒,化工厂常用浓氨水检测氯气储存设备或者输气管是否有氯气泄漏。A、B、C、D表示4种物质,其微观示意图见下表,A和B在一定条件下反应生成C和D。
物质 | A | B | C | D |
|
化学式 | NH3 | Cl2 | N2 | ||
微观示意图 |
|
|
|
|
D的化学式为 。
若17 g A参加反应,则生成C的质量为 g。
【答案】(1)氢气 2H2O通电2H2↑+ O2↑ (2) CaO + H2O === Ca(OH)2
(3)9:25 (4)400g (5)① HCl ②14
【解析】
试题分析:(1) 电解水实验口诀:正氧负氢,氢二氧一,即与电源正极相连产生的是氧气,与电源负极相连产生的是氢气,所以试管1产生的气体是氢气,反应的化学方程式:2H2O通电2H2↑+ O2↑
(2) 生石灰与水反应的化学方程式为:CaO + H2O === Ca(OH)2
(3) 20℃时,氯化钠的溶解度为36g,意思是在20℃时,100g水中达到饱和状态最多溶解氯化钠的质量为36g,所以20℃时氯化钠饱和溶液中溶质和溶剂的质量比=36:100=9:25
(4) 将200g30%的氯化钠溶液稀释为10%的氯化钠溶液,稀释过程中溶质的质量不变,可设需水的质量为x,列式为:200g×30%=(200g+x)×10%,x=400g
(5)①根据微观示意图,可D的化学式为HCl,②所以该反应的化学方程式:2NH3+3Cl2=N2[来+6 HCl,根据方程式中A和C的质量关系34:28,所以若17 g A参加反应,则生成C的质量为14g

【题目】(8分)氢氧化钠与盐酸的反应无明显现象,某化学兴趣小组为证明氢氧化钠与盐酸发生了化学反应,进行了如下的实验探究。
【实验探究一】小云在试管中加入约2mL稀氢氧化钠溶液,滴入2滴酚酞溶液,振荡,溶液变为红色。然后向该试管中滴加稀盐酸,观察到溶液 ,证明氢氧化钠与盐酸发生了反应,该反应的化学方程式为 。
【反思评价】 小霞提出也可以使用石蕊试液代替无色酚酞进行上述实验。你认为 (填“无色酚酞”或“石蕊试液”)更适合用于验证二者恰好完全反应,你的理由是 。
【实验探究二】小兰同学将不同浓度的盐酸和NaOH溶液各10 mL混合,用温度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如下表)。
编号 | 盐酸 | NaOH溶液 | △t/℃ |
1 | 3.65﹪ | 2.00﹪ | 3.5 |
2 | 3.65﹪ | 4.00﹪ | x |
3 | 7.30﹪ | 8.00﹪ | 14 |
表中x = 。
【反思评价】某同学在没使用温度计的情况下,通过右图所示装置完成了实验。则该同学根据
判断NaOH溶液与稀盐酸发生了中和反应。但有同学认为单凭此现象不足以说明该反应放热,其理由是 。
【拓展延伸】不是所有的碱与盐酸反应都无明显现象,例如 (填一种碱)与盐酸反应就有明显的实验现象。