��Ŀ����
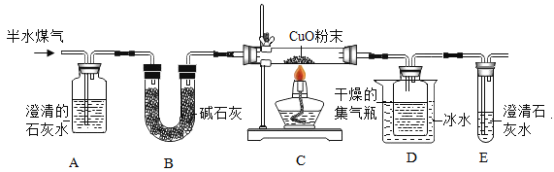
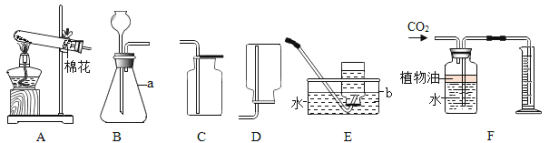
����Ŀ��ʵ��С���ͬѧ��ʵ������ѡ������װ�ã�̽������������ȼ�յ�ʵ��
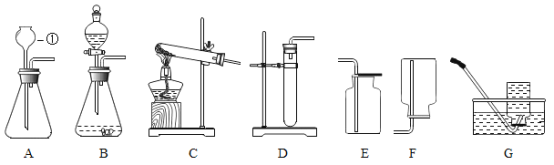
��1��д��ͼ�б�����������ƣ���_____��
��2��С��ͬѧѡ������غͶ���������ȡ��������ѡ��ķ���װ����_____(����ĸ��ţ���ͬ)���ռ�����������,ѡ��_____��д���÷�Ӧ�Ļ�ѧʽ��Ӧʽ_____��
��3��С��ͬѧѡ�ø��������ȡ������д���÷�Ӧ�Ļ�ѧʽ����ʽ��_____���Թܿ���������б������Ϊ_____��
��4��С��۲쵽����������ȼ�յ�������_____(����) ��
��5��Сͭͬѧ����п��ϡ���ᷴӦ,��������ȡ����,��������Ũ���Դ�,��Ӧ�dz�����,��Ӧѡ��ķ���װ����_____�����ռ����������,ѡ�õ��ռ�װ����_____��
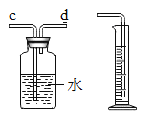
��6��С�����ռ���ƿ����,��Ƶ��ռ�װ����ͼ��ʾ��������_____�˽��루����ţ�,װ���ڵĿ����Բ������_____�����Ӱ�족����Ӱ�족����
��7��С���ʵ����з�˼����Щ���ؾ�������װ������_____����Щ���ؾ����ռ�װ������_____��
���𰸡�����©�� C G 2KClO3![]() 2KCl+3O2�� 2KMnO4
2KCl+3O2�� 2KMnO4![]() K2MnO4+MnO2+O2�� ��ֹ����ˮ������ʹ���ȵ��Թ�ը�� ��������ɫ���棬�����д̼�����ζ���� B F d ��Ӱ�� ��Ӧ���״̬�뷴Ӧ���� ������ܽ������ܶ�
K2MnO4+MnO2+O2�� ��ֹ����ˮ������ʹ���ȵ��Թ�ը�� ��������ɫ���棬�����д̼�����ζ���� B F d ��Ӱ�� ��Ӧ���״̬�뷴Ӧ���� ������ܽ������ܶ�
��������
��1�����dz���©�����������©����
��2����������������������Ҫ���ȣ�Ӧѡ�õķ���װ����Cװ�ã�������ڶ��������������ͼ��ȵ������������Ȼ��غ���������Ӧ�Ļ�ѧ����ʽ�ǣ�2KClO3![]() 2KCl+3O2������ˮ���ռ���������Ϊ������
2KCl+3O2������ˮ���ռ���������Ϊ������
���C��G��2KClO3![]() 2KCl+3O2����
2KCl+3O2����
��3����������ڼ��ȵ���������������ء��������̺���������ѧ����ʽΪ��2KMnO4![]() K2MnO4+MnO2+O2�����Թܿ���������б��Ŀ���ǣ���ֹ����ˮ������ʹ���ȵ��Թ�ը�ѣ�
K2MnO4+MnO2+O2�����Թܿ���������б��Ŀ���ǣ���ֹ����ˮ������ʹ���ȵ��Թ�ը�ѣ�
���2KMnO4![]() K2MnO4+MnO2+O2������ֹ����ˮ������ʹ���ȵ��Թ�ը�ѣ�
K2MnO4+MnO2+O2������ֹ����ˮ������ʹ���ȵ��Թ�ը�ѣ�
��4������������ȼ�յ������ǣ���������ɫ���棬�����д̼�����ζ���壻
�����������ɫ���棬�����д̼�����ζ���壻
��5����п��ϡ���ᷴӦ����������ȡ������Ӧ��ѡ��B����ΪB�ܿ��Ʒ�Ӧ���ʣ��������ܶ�С�ڿ��������ռ������������ѡ�õ��ռ�װ����F��
���B��F��
��6��С�����ռ���ƿ����,��Ƶ��ռ�װ����ͼ��ʾ���������ܶ�С��ˮ����d�˽��루����ţ�,װ���ڵĿ����Բ�����������������Ӱ�죻
���d����Ӱ�죻
��7������������ѡ��C�������Һ�岻����ѡ��A��B��D�����岻����ˮ��������ˮ���ռ����ܶȱȿ������������ſ������ռ����ܶȱȿ���С�����������ſ������ռ����ʴ�Ϊ����Ӧ���״̬�뷴Ӧ������������ܽ������ܶȡ�