题目内容
【题目】近年来,我国航天、航空、高铁等得到长足发展,跻身世界前列。大飞机C919试飞成功,标志着我国航天梦又迈出一大步。大飞机使用的材料如图:
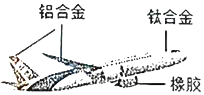
(1)机头外壳用到了钛合金,构成金属钛的粒子是_____(填“原子”“分子”或“离子”),工业制钛有一种反应为:TiF4+2H2SO4![]() 4HF+2X+TiO2,X的化学式为_____。
4HF+2X+TiO2,X的化学式为_____。
(2)机翼和机尾用到了铝合金。铁的强度比铝大,但是制作飞机外壳却不用铁合金,主要原因是铝的密度比铁小且耐腐蚀性强,铝具有很好的抗腐蚀性能的原因是_____。
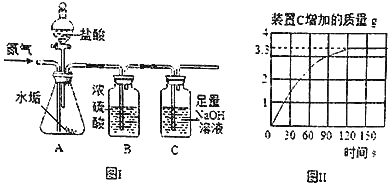
(3)小刚查资料发现航母中也用到金属钛,同时还用到锌、铁、铜三种金属。他想探究锌、铁、铜三种金属的活动性强弱,小刚设计了下列实验:向稀盐酸中依次加入足量铁片,充分反应后再加铜片,最后加入锌片。该实验能确定锌的活动性最强的实验现象是_____。写出实验过程中所发生的所有的化学方程式_____。
【答案】原子 【答题空2】SO3 铝和空气中的氧气反应生成致密的氧化铝薄膜,阻碍铝的进一步反应 锌表面会析出银白色固体,浅绿色溶液逐渐变为无色 【答题空5】Fe+2HCl=FeCl2+H2↑、Zn+FeCl2=ZnCl2+Fe
【解析】
(1)建造航母用到了钛合金,构成金属钛的粒子是原子,故填原子;工业制钛有一种反应为TiF4+2H2SO4![]() 4HF+2X+TiO2,由质量守恒定律反应前后原子的种类及数目不变可知,反应物中有1个钛原子,4个氟原子,4个氢原子,2个硫原子,8个氧原子,生成物中含有4个氢原子,4个氟原子,1个钛原子,2个氧原子,所以X的化学式为SO3,故填SO3;
4HF+2X+TiO2,由质量守恒定律反应前后原子的种类及数目不变可知,反应物中有1个钛原子,4个氟原子,4个氢原子,2个硫原子,8个氧原子,生成物中含有4个氢原子,4个氟原子,1个钛原子,2个氧原子,所以X的化学式为SO3,故填SO3;
(2)铝和空气中的氧气反应生成致密的氧化铝薄膜,阻碍铝的进一步反应,所以铝具有很好的抗腐蚀性能,故填铝和空气中的氧气反应生成致密的氧化铝薄膜,阻碍铝的进一步反应;
(3)稀盐酸中加入足量铁粉后,生成了浅绿色的氯化亚铁和氢气,再加铜粉不反应,说明了铁的金属活动性大于铜,最后加入锌粉,锌能和氯化亚铁反应将铁置换出来,同时生成氯化锌,说明了锌的活动性大于铁,可以比较金三种属的活动性强弱,故填锌表面析出银白色固体,溶液由浅绿色逐渐变为无色;发生的化学反应方程式故填Fe+2HCl=FeCl2+H2↑、Zn+FeCl2=ZnCl2+Fe。

【题目】对比实验是实验探究的重要方法,下列对比实验设计能实现相应实验目的是( )
选项 | 实验目的 | 实验设计 | 选项 | 实验目的 | 实验设计 |
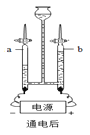
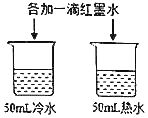
A | 探究温度对分 子运动快慢的影响 |
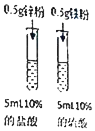
| B | 探究金属活动性 强弱 |
|
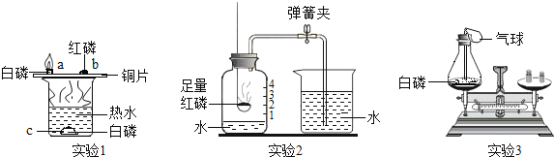
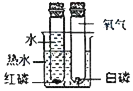
C | 探究氧气是燃烧 的必要条件 |
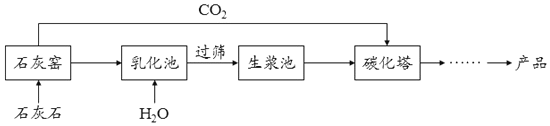
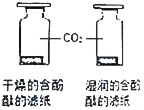
| D | 探究CO2与水 发生反应 |
|
A. A B. B C. C D. D