题目内容
【题目】长期使用的热水壶底部有一层水垢,水垢主要成分是碳酸钙和氢氧化镁和少量杂质(杂质不溶于水也不与酸反应)。某研究性学习小组为测定水垢中碳酸钙的质量分数,利用图I装置将足量的盐酸加入到10.0g水垢中。随反应进行,装置C质量的变化如图Ⅱ所示。请回答: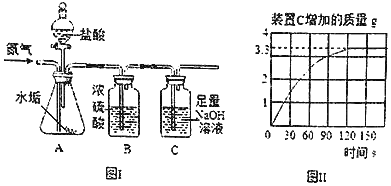
(1)反应结束后总共生成二氧化碳的质量是_____g;
(2)若各装置内均恰好完全反应且不考虑盐酸的挥发,请根据图Ⅱ数据计算,水垢中碳酸钙的质量分数是多少_____?(写出具体计算过程)
(3)反应后向装置内通入氮气是为了让测量更准确,如果省略这一步骤会使得最终得到的结果_____。(填“偏大”或“偏小”或“无影响”)。
(4)根据以上探究过程,下列说法正确的是_____。
A.根据本题的数据还可以求出氢氧化镁在水垢中的质量分数
B.如果实验过程中逐滴滴加10%盐酸至恰好不再产生气泡,恰好消耗的盐酸溶液质量为m,再结合本题数据可求出氢氧化镁在水垢中的质量分数
C.本实验还可以通过实验后过滤、洗涤并干燥滤渣,称量滤渣质量来求出碳酸钙的质量分数
【答案】3.3; 75%。 偏小。 B
【解析】
(1)根据图Ⅱ可以看出生成的二氧化碳的质量为3.3g;
(2)若各装置内均恰好完全反应且不考虑盐酸的挥发,根据图Ⅱ生成二氧化碳质量进行计算,设水垢中碳酸钙的质量分数为x,

![]() =
=![]() 解得x=75%,答:水垢中碳酸钙质量分数为75%,故填75%;
解得x=75%,答:水垢中碳酸钙质量分数为75%,故填75%;
(3)反应后向装置内通入氮气是为了让测量更准确,如果省略这一步骤,导致二氧化碳不能完全被C装置吸收,导致C装置的变化量偏小,二氧化碳质量偏小,会使得最终得到的结果偏小,故填偏小;
(4)
A、根据本题的数据,由于还含有杂质,所以不能求出氢氧化镁在水垢中的质量分数,故选项不正确;
B、如果实验过程中逐滴滴加10%盐酸至恰好不再产生气泡,恰好消耗的盐酸溶液质量为m,再结合本题数据可求出氢氧化镁在水垢中的质量分数,具体过程为:根据二氧化碳的质量可以求算与碳酸钙反应的盐酸,进而确定与氢氧化镁反应的盐酸的质量,根据与氢氧化镁反应的盐酸的质量和对应的化学方程式求算氢氧化镁的质量或者直接求算氢氧化镁在水垢中的质量分数,故选项正确;
C、滤渣中还有氢氧化镁和盐酸反应生成的氯化镁,所以不能用这种方法求出碳酸钙的质量分数,故选项不正确,故填B。

 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案