题目内容
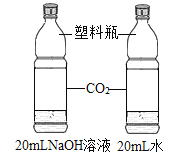
【题目】某化学活动小组在一次实验中进行如图所示实验:
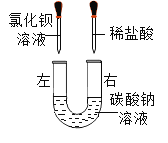
此时观察到 U 型管左右两侧产生的现象分别是 _____;实验后,小组同学充分振荡 U 型管, 发现管内仍有白色固体残留,将混合物过滤后,同学们对滤液成分产生了浓厚的兴趣,于是进行了进一步的探究活动。
(提出问题):滤液中可能含有哪些溶质?
(猜想与假设)猜想一:溶质为 NaCl
猜想二:溶质为 NaCl 和 BaCl2
猜想三:溶质为 NaCl、BaCl2和 HC1
(评价与交流):你认为以上猜想 _____不合理,理由是 _____;则你的猜想为 _____;
(实验探究)小红为了验证滤液成分,取滤液于试管中,向其中滴加少量的硫酸钠溶液,观察到无明显现象。由此得出结论:猜想一成立,小刚认为小红的结论不严密,因为 _____。
为验证你的猜想请填写如表
实验过程 | 实验现象 | 实验结论 |
_____ | _____ | 你的猜想成立 |
【答案】左侧产生白色沉淀,右侧产生气泡 三 当U型管内仍有白色沉淀时,溶液中的HCl一定完全反应 NaCl、Na2CO3 该现象只能证明溶液中不含氯化钡,无法证明溶液中是否含有碳酸钠 取少量滤液于试管中,向其中滴加少量的稀盐酸 有气泡产生
【解析】
向左侧滴入氯化钡溶液,氯化钡与碳酸钠反应生成碳酸钡沉淀和氯化钠,有白色沉淀产生,向右侧滴加稀盐酸,碳酸钠与稀盐酸反应生成氯化钠、二氧化碳和水,有气泡产生,故U 型管左右两侧产生的现象分别是:左侧产生白色沉淀,右侧产生气泡;
评价与交流:以上猜想三不合理,理由是U型管内仍有白色固体残留,如果滤液中含有盐酸,盐酸会与碳酸钡反应,不可能共存;
向左侧滴入氯化钡溶液,氯化钡与碳酸钠反应生成碳酸钡沉淀和氯化钠,向右侧滴加稀盐酸,碳酸钠与稀盐酸反应生成氯化钠、二氧化碳和水,故滤液中一定含有氯化钠、可能含有氯化钡或碳酸钠中的一种,故猜想为:NaCl、Na2CO3;
实验探究:小红为了验证滤液成分,取滤液于试管中,向其中滴加少量的硫酸钠溶液,观察到无明显现象,说明滤液中不含氯化钡,但是无法证明不含碳酸钠,故不能证明猜想一成立;
为了验证滤液中含有NaCl、Na2CO3,可取少量滤液于试管中,向其中滴加少量的稀盐酸,稀盐酸能和碳酸钠反应生成氯化钠、二氧化碳和水,如果有气泡产生,则证明含有碳酸钠。
故实验操作为:取少量滤液于试管中,向其中滴加少量的稀盐酸,实验现象为:有气泡产生。

 阅读快车系列答案
阅读快车系列答案【题目】将20g稀盐酸逐滴加入装有40g质量分数为10%的氢氧化钠溶液的烧杯中,随着稀盐酸滴加,杯内溶液pH变化如图所示,温度变化如表所示(不考虑反应过程中热量散失)。

反应时间(s) | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
溶液温度(℃) | 20.5 | 20.6 | 20.7 | 20.8 | 20.9 | 20.8 | 20.7 |
(1)当稀盐酸与氢氧化钠溶液恰好完全反应时,溶液的温度是 ℃。
(2)计算恰好完全反应时,所得溶液溶质质量为多少?
【题目】设计对比实验,控制变量是学习化学的重要方法,下列对比实验不能达到目的的是
编号 | ① | ② | ③ | ④ |
实验设计 |
|
|
|
|
实验目的 | 探究同种物质在不同溶剂中的溶解性 | 探究可燃物燃烧的条件 | 探究铁生锈的条件 | 探究CO2与NaOH溶液能否发生反应 |
A.AB.BC.CD.D