题目内容
【题目】实验室欲制备二氧化碳。
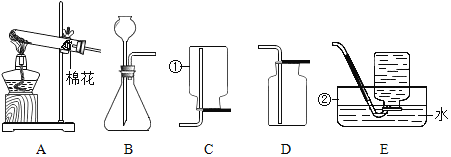
(1)市售浓盐酸的标签局部见图,标签中“36%”的含义是_________________。为使制备过程中二氧化碳平稳地产生且较纯净,应将该浓盐酸稀释。

(2)宜选择的固体药品是__________________ (选填编号)。
a 粉末状石灰石
b 块状大理石
c 粉末状熟石灰
d 块状生石灰
(3)为方便地控制反应的发生或停止,发生装置应选用____________(选填编号),仪器P的名称是_________________。

(4)若用D装置收集二氧化碳时,气体从______________ (选填“m”或“n”)端进入。.
(5)反应生成了0.15mo1二氧化碳,求参与反应的HCl的质量______________。 (根据化学方程式列式计算)
【答案】每100g盐酸溶液中含36g氯化氢 b A 长颈漏斗 n 10.95g
【解析】
(1)标签中百分数,表示溶液中溶质质量分数,所以36%是指每100g盐酸溶液中含有36g氯化氢;
故答案为:每100g盐酸溶液中含36g氯化氢。
(2)a、粉末状石灰石与盐酸接触面积较大,反应速率较快,不利于气体收集,选项a不符合题意;
b、块状石灰石与盐酸接触面积适中,反应速率较平缓,利用气体收集,选项b符合题意;
c、熟石灰与盐酸反应生成氯化钙和水,不生成二氧化碳,不能制备气体,选项c不符合题意;
d、生石灰与盐酸反应生成氯化钙和水,不生成二氧化碳,不能制备气体,选项d不符合题意;
故答案为:b。
(3)为方便地控制反应的发生或停止,需要能够控制固液接触,A中关闭止水夹,气体增多,内部压强增大,将液体通过多孔隔板将液体压入长颈漏斗,固液分离,反应停止,打开止水夹,气体输出,压强减小,液体重新进入试管,固液接触,反应发生,因此A可以控制反应的发生或停止;P为加入液体的长颈漏斗;
故答案为:A;长颈漏斗。
(4)二氧化碳密度比空气大,进入瓶内,先在底部聚集,所以从长口n进气,从短口m排气,达到收集气体目的;
故答案为:n。
(5)设参加反应的氯化氢为x mol,
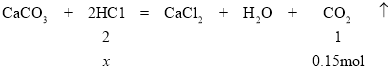
![]() x=0.3mol
x=0.3mol
氯化氢的质量=![]()
故答案为:10.95g。

 名校课堂系列答案
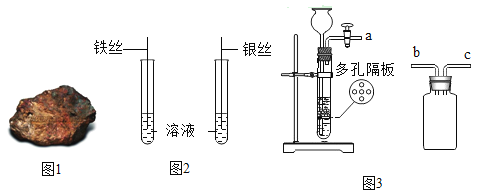
名校课堂系列答案【题目】某化学兴趣小组的同学在探究金属的有关性质时,进行了如图所示实验:在A实验结束后将两支试管内的物质倒入一洁净烧杯中,一段时间后过滤 。为确定过滤后得到的滤渣和滤液的成分,同学们进行了如下实验。

实验一:滤渣的成分是什么?
(1)甲同学取少量滤渣于试管中,加入稀硫酸,无气泡产生,证明滤渣里不含_________,乙同学通过物理方法也得到同样的结论,请简述其方法和现象:_________。
实验二:滤液里的溶质有哪些?
(2)同学们一致认为定有FeSO4,为确定可能含有其他溶质,同学们进行了如下实验:
实验步骤 | 实验现象 | 实验结论 |
取少量滤液,向其中加入足量铝粉 | 产生气泡,并有红色固体析出 | 滤液里的溶质还有_______ |
请写出产生气泡反应的化学方程式:_________。
(3)有同学提出可以直接观察滤液的颜色判断滤液中是否含有硫酸铜,同学们对硫酸铜溶液为什么呈蓝色很感兴趣,决定探究硫酸铜溶液中哪种粒子使溶液呈蓝色。设计的实验方案如下:
实验操作 | 实验现象 | 实验结论 |
①取少量_______溶液,观察颜色 | 溶液呈无色 | 硫酸根离子不能使溶液呈蓝色 |
②取少量硫酸铜溶液,观察颜色 | 溶液呈蓝色 | 铜离子使溶液呈蓝色 |
(4)除了(3)中的实验方案外,你还能设计其他方案探究硫酸铜溶液中是铜离子使溶液呈蓝色吗?实验所需的药品和仪器任选,请简述实验操作和实验现象。
实验操作:___________。
实验现象:____________。