题目内容
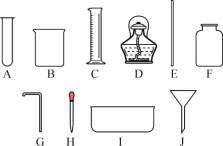
【题目】化学是一门以实验为基础的科学,请结合图示回答问题:
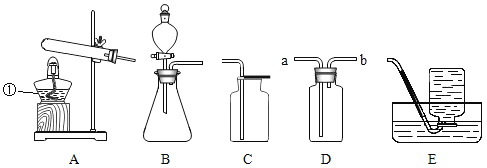
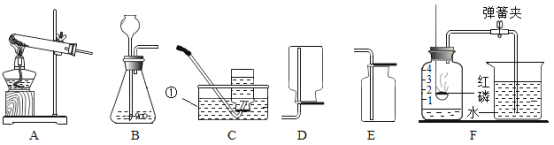
(1)图中仪器①的名称是_____.
(2)实验室用高锰酸钾制取氧气的化学反应方程式为 _____。
(3)实验室制取二氧化碳,选择发生装置B,其优点是_____ 。该反应的化学方程式为_____。
(4)实验室中常用氯化铵和熟石灰的固体混合物加热制取氨气.通常状况下,氨气是一种无色、有刺激性气味的气体,极易溶于水,密度比空气小.实验室欲制取氨气,可选择的发生装置是_____(填序号),若用装置D收集一瓶氨气,则氨气应从_____(填“a”或“b”)端通入,多余的氨气应进行处理,防止污染环境.
(5)某些大理石中含少量硫化物,使制得的CO2中混有H2S气体。欲获取纯净、干燥的CO2,需对发生装置中产生的气体进行除杂,实验装置如下:
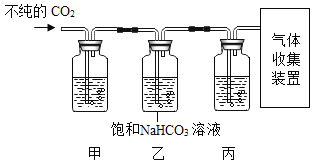
查阅资料:I.H2S能与NaOH等碱溶液、CuSO4溶液反应。
Ⅱ.CO2中混有的HC1气体可用饱和NaHCO3溶液吸收。
装置甲中所盛试剂应选用_____(填字母)。
A 浓硫酸 B NaOH溶液 C 澄清石灰水 D CuSO4溶液
【答案】酒精灯 2KMnO4![]() K2MnO4+MnO2+O2↑ 可以控制反应速度(速率)的快慢 CaCO3+2HCl=CaCl2+H2O+CO2↑ A b D
K2MnO4+MnO2+O2↑ 可以控制反应速度(速率)的快慢 CaCO3+2HCl=CaCl2+H2O+CO2↑ A b D
【解析】
(1)由图可知,图中仪器①的名称是酒精灯;
(2)实验室用高锰酸钾制取氧气,生成物除了氧气,还有锰酸钾和二氧化锰,化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3) 装置B有分液漏斗,可以控制液体的滴加速度,进而控制反应速度(速率)的快慢,故填写:可以控制反应速度(速率)的快慢;
实验室制取二氧化碳,利用大理石和稀盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(4)实验室中常用氯化铵和熟石灰的固体混合物加热制取氨气,发生装置选择带酒精灯的装置,即A,故填写:A;
氨气是密度比空气小,若用装置D收集一瓶氨气,则氨气应从b端进入,故填写:b;
(5)制得的CO2中可能混有H2S、HCl、H2O,由题干可知,CO2中混有的HC1气体可用饱和NaHCO3溶液吸收,装置甲内试剂是用于除H2S的,NaOH溶液和澄清石灰水与二氧化碳反应,不能用于除杂,浓硫酸过量时与硫化氢反应产生二氧化硫,引入新的杂质,硫酸铜可与硫化氢反应生成硫化铜沉淀和硫酸,故D选项符合题意,填写:D。

【题目】如图是某班进行的“空气中氧气含量测定”的分组实验.
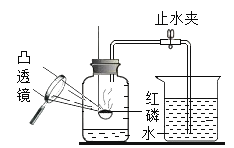
下面是某组凌乱的实验步骤记录:
①待集气瓶完全冷却至室温,打开止水夹;
②用凸透镜聚集阳光照射红磷;
③在集气瓶里加入适量的水,燃烧匙里放一小块红磷;
④红磷燃烧熄灭后,进行震荡;
⑤连接仪器,检查装置的气密性;
⑥计算出空气中氧气的体积分数.
(1)上述实验正确的步骤为__________________.(填写序号)
(2)红磷燃烧时,火焰呈黄色,同时产生浓厚的________.请写出红磷燃烧的文字表达式________。
(3)下表为该班的6个实验小组测定的数据:(集气瓶的容积为100mL,已扣除实验前加入的水量)
组别 | 1 | 2 | 3 | 4 | 5 | 6 |
进入集气瓶中水的体积/mL | 15 | 21 | 19 | 22 | 30 | 20 |
分析实验数据,从第2、3、4、6组验证出氧气约占空气体积的_____.(填百分比)
第1组出现较大偏差的原因可能是______________;
第5组出现较大偏差的原因可能是_____________