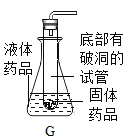
��Ŀ����
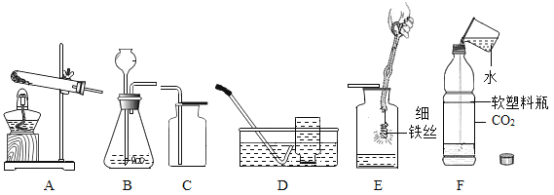
����Ŀ��ijͬѧΪ̽��һƿ��ɫҺ��A�ijɷ֣���������ʵ�飺
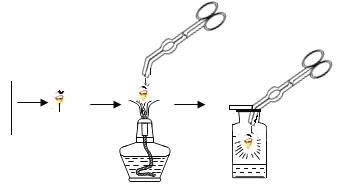
����A�м����ɫ��ĩB���ڳ����¾���Ѹ�ٲ�������C��ͬʱ�����˳�����ΪҺ��Ĵ�����D����B�������ͻ�ѧ�����ڷ�Ӧǰ��û�иı䣮
�ڸ�ͬѧ������C�ռ��������������ǵ�ľ������ʢ��C�ļ���ƿ�У�ľ������ȼ�գ�
�����⽫��ɫ��ĩE��ȼ�����ʢC�ļ���ƿ�У��ܾ���ȼ�գ�����һ����ɫ���д̼�����ζ������F��������ݸ�ͬѧ��ʵ��ش����⣺
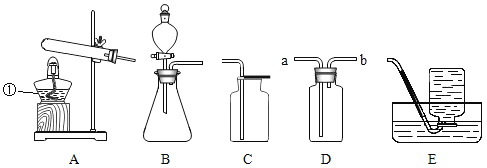
��1��д���������ʵ����ƣ�B______��D______��
��2��д��A��B�õ�C��D�����ֱ���ʽ______��
��3��д��E+C��F�����ֱ���ʽ��______��
���𰸡��������� ˮ ��������![]() ˮ+���� ��+����
ˮ+���� ��+����![]() ��������
��������
��������
������C�ռ��������������ǵ�ľ������ʢ��C�ļ���ƿ�У�ľ������ȼ�գ���C����������A�м����ɫ��ĩB���ڳ����¾���Ѹ�ٲ�������C��ͬʱ�����˳�����ΪҺ��Ĵ�����D����B�������ͻ�ѧ�����ڷ�Ӧǰ��û�иı䣬��B�ڸ÷�Ӧ���������������ѧ֪ʶ��B�Ƕ������̣�A�ǹ������⣬D��ˮ�����⽫��ɫ��ĩE��ȼ�����ʢC�ļ���ƿ�У��ܾ���ȼ�գ�����һ����ɫ���д̼�����ζ������F����E����F�Ƕ�����������֤��ȷ��
��1��B�Ƕ������̣�D��ˮ��
��2��A��B�õ�C��D�����ֱ���ʽ�ǣ���������![]() ˮ+������
ˮ+������
��3��E+C��F�����ֱ���ʽ�ǣ���+����![]() ��������
��������

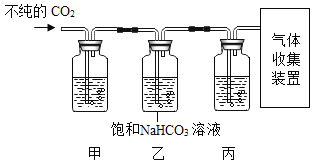
����Ŀ���ڸ����£�����ˮ�����ܷ�����Ӧ����һ�ֳ����������������һ�����塣ij��ȤС����������о�������ˮ������Ӧһ��ʱ���ʣ��������ʵijɷ֡����ʼ������á�
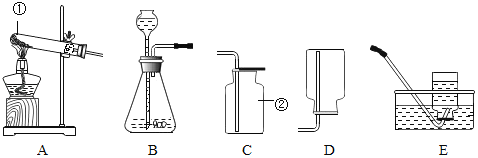
ʵ��װ����ͼ��ʾ(�г�������)
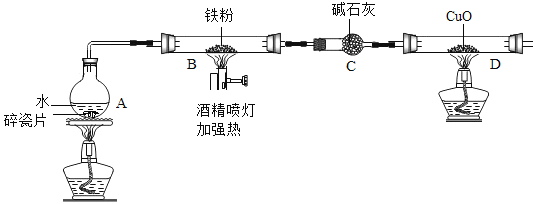
(1)���ƶϣ��۲쵽D�к�ɫ�����죬��B�����ɵ�������_____________��
(2)̽��Bװ����ʣ�����ɷ���ʲô��
���������ϣ�
��1�������Ƭ�ܷ����У���ʯ���������ƺ��������ƵĻ����
��2���������������У�ֻ��Fe2O3�Ǻ���ɫ�������Ϊ��ɫ��ֻ��Fe3O4�ܱ�����������
������̽����
Bװ����ʣ�����Ϊ��ɫ����ȫ��������������
����������裩
����һ��ʣ�������Fe3O4��
�������ʣ�������_____________��
��ʵ��̽����
ʵ����� | ʵ�������� |
ȡ������ɫ�������Թ��У�����������ϡ����(��ϡ����) | ������ȫ���ܽ⣬û������ð����ʣ�������Fe3O4��������ȫ���ܽ⣬������ð����ʣ�������Fe��Fe3O4(��ʵ�����һ��) |
��ʵ����ۣ�����ˮ������Ӧ�Ļ�ѧ����ʽΪ_____________��
(3)���ɷ������ã�����Bװ����ʣ��ĺ�ɫ����a g������һϵ��ת����ȫ����Ϊ����ɫ����Fe2O3(����ת����������Ԫ�������)�����ӵ�����Ϊx����x��ȡֵ��ΧΪ_____________��
����Ŀ������˵����ȫ��ȷ���ǣ�������
A | �����Ļ�ѧʽ���� 1����ԭ�ӡ��� 1��������--- | B | ����Ԫ�����ࡪ�������� ����Ԫ�ػ�ѧ���ʡ������������� ����Ԫ�������ڱ��е����������������Ӳ��� |
C | �������ɷ��ӹ��� ������̼������ԭ�ӹ��� ����ͭ���������ӹ��� | D | ���ӡ�����ѧ�仯�е���С���� ԭ�ӡ����������ʻ�ѧ���ʵ���С���� ���ӡ��������ԭ�ӻ�ԭ���� |
A. AB. BC. CD. D