题目内容
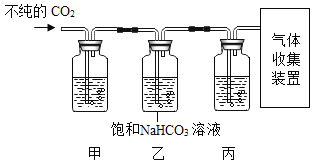
【题目】下图是电解水的简易装置:
(1)请在图示括号中用“+”“-”号标出正负极。______________ _______

(2)与电源正极相连的试管内产生的气体能______________,这是_______气;与电源负极相连的试管内产生的气体可以______,这是____气。若正极收集到气体10mL,则负极可以收集到气体_____mL。这一变化的文字表达式为_________________________,属于基本反应类型中的_______反应。
(3)做该实验需向水中加入少量的稀硫酸和氢氧化钠溶液,其目的是_______
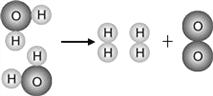
(4)下图是水分子分解示意图,请回答下列问题:该实验过程中,发生变化的微粒是 ___________,没有发生变化的微粒是_______________,此实验验证了在化学变化中______能分,而_______不能分。
【答案】 + — 使带火星的木条复燃 氧气 燃烧 氢气 20 水![]() 氢气+氧气 化合 【答题空10】增加水的导电性 水分子 氢原子和氧原子 分子 原子
氢气+氧气 化合 【答题空10】增加水的导电性 水分子 氢原子和氧原子 分子 原子
【解析】(1)由电解水的实验装置可知,左侧试管收集的气体较少是氧气,所连接的是电源的正极,则右边是负极,见下图: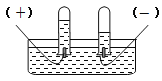 ;
;
(2)与电源正极相连的试管内产生的气体是氧气具有助燃性,能使带火星的木条复燃;与电源负极相连的试管内产生的气体可以燃烧,这是氢气;若正极收集到气体10mL,则负极可以收集到气体20mL;这一变化的文字表达式为:水![]() 氢气+氧气,符合“一变多”的特点,属于基本反应类型中的分解反应;
氢气+氧气,符合“一变多”的特点,属于基本反应类型中的分解反应;
(3)做该实验需向水中加入少量的稀硫酸和氢氧化钠溶液等,其目的是增加水的导电性;
(4)图2是水分子分解示意图,请回答下列问题:由微粒IDE变化可知该实验过程中,发生变化的微粒是水分子,没有发生变化的微粒是 氢原子和氧原,此实验验证了在化学变化中分子能分,而原子不能分。

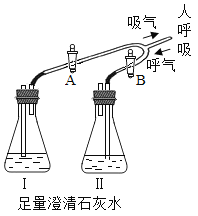
【题目】在高温下,铁与水蒸气能发生反应生成一种常见的铁的氧化物和一种气体。某兴趣小组请你参与研究:铁与水蒸气反应一段时间后剩余固体物质的成分、性质及再利用。
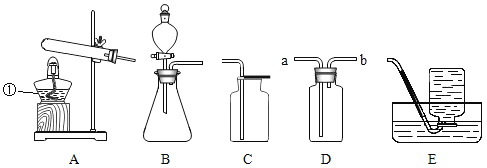
实验装置如图所示(夹持仪器略)
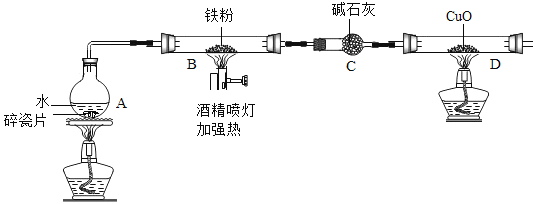
(1)(推断)观察到D中黑色固体变红,则B中生成的气体是_____________。
(2)探究B装置中剩余固体成分是什么?
(查阅资料)
(1).碎瓷片能防爆沸;碱石灰是氧化钙和氢氧化钠的混合物
(2).铁的氧化物中,只有Fe2O3是红棕色,其余均为黑色,只有Fe3O4能被磁铁吸引。
(初步探究)
B装置中剩余固体为黑色,能全部被磁铁吸引。
(猜想与假设)
猜想一:剩余固体是Fe3O4;
猜想二:剩余固体是_____________。
(实验探究)
实验操作 | 实验现象及结论 |
取少量黑色固体于试管中,加入足量的稀盐酸(或稀硫酸) | 若固体全部溶解,没有气泡冒出,剩余固体是Fe3O4,若固体全部溶解,有气泡冒出,剩余固体是Fe和Fe3O4(与实验操作一致) |
(实验结论)铁与水蒸气反应的化学方程式为_____________。
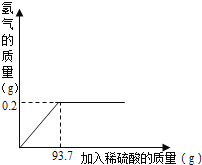
(3)(成分再利用)若将B装置中剩余的黑色固体a g,经过一系列转化,全部变为红棕色固体Fe2O3(假设转化过程中铁元素无损耗),增加的质量为x,则x的取值范围为_____________。