题目内容
【题目】下图是芸芸(甲)、绪绪(乙)两位同学一起在实验室进行的氢氧化钠与盐酸中和反应的实验。
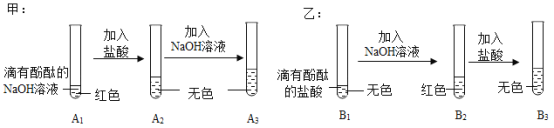
(说明:图中 A1、A2、A3、B1、B2、B3 均为溶液编号) 根据上图实验,请你与芸芸、绪绪同学一起完成下列探究:
探究环节 | 芸芸同学的探究 | 绪绪同学的探究 |
提出问题 | A3 溶液为什么不变红? | B3 溶液中溶质成分是什么?(酚酞不计) |
作出猜想 | 实验过程中,酚酞变质了。 | 猜想一:NaCl 猜想二:NaCl、HCl |
实验验证 | (1)取少量 A3 溶液于另一试管中,向其中滴 加 NaOH 溶液,溶液变红,说明芸芸同学的 猜想_____(填“成立”或“不成立”)。 (2)你认为,在常温下 A2 溶液测出的 pH 应_____(填“>”、“=”或“<”)7。 | 取少量 B3 溶液加入盛有少量铁粉的试管 中,观察到有无色气泡产生,固体逐渐减 少,溶液由无色变为_____。据此,你 认为绪绪同学的猜想_____(填“一”或 “二”)成立。 |
交流反思 | (1)芸芸、绪绪同学的实验中,反应均涉及到的化学方程式是_____。 (2)A3 溶液未变红,你认为原因是 A2 溶液中_____较多,加入的 NaOH 溶液 未将其完全中和。 (3)芸芸、绪绪同学经过实验对比探究,一致认为做化学实验时应注意药品用量的控制。 | |
【答案】不成立 < 浅绿色 二 NaOH+HCl=NaCl+H2O 盐酸
【解析】
实验验证:芸芸同学的探究:(1)取少量 A3 溶液于另一试管中,向其中滴 加 NaOH 溶液,溶液变红,说明酚酞没有变质,而是氢氧化钠加少了,说明芸芸同学的猜想不成立。故填:不成立。
(2)A1加入盐酸后溶液由红色变为无色,此时A2溶液可能为中性,液可能为酸性,A2溶液加入氢氧化钠之后,仍为无色,说明加入的盐酸过量,此时溶液是酸性,A2 溶液测出的 pH应<7。故填:<。
绪绪同学的探究:取少量 B3 溶液加入盛有少量铁粉的试管中,观察到有无色气泡产生,说明盐酸有剩余,固体逐渐减少,是因为铁和盐酸发生了反应生成氢气和氯化亚铁,溶液由无色变为浅绿色。据此,绪绪同学的猜想二成立。故填:浅绿色;二。
交流反思:(1)芸芸、绪绪同学的实验中,反应均涉及到的反应是氢氧化钠和盐酸发生中和反应生成氯化钠和水,其化学方程式为: NaOH+HCl=NaCl+H2O;故填:NaOH+HCl=NaCl+H2O。
(2)由于A3溶液不呈碱性,因此A3溶液未变红,原因是A2溶液中盐酸较多,加入的NaOH溶液未将其完全中和。故填:盐酸。

 阅读快车系列答案
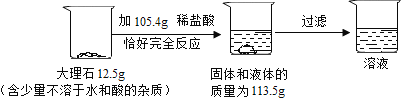
阅读快车系列答案【题目】做完加热铜片的实验后,小明同学对其成分进行分析。取10g此样品,向其中分五次加入相同溶质质量分数的稀硫酸,使之充分反应,每次所用稀硫酸的质量及剩余固体的质量记录于下表:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 | 20 |
充分反应后剩余固体的质量/g | 9.2 | 8.4 | 7.6 | 7 | 7 |
试回答下列问题:
(1)10g样品中氧化铜的质量为__________g。
(2)计算所加入稀硫酸中溶质的质量分数____________________。
【题目】下列图象能正确反映对应变化关系的是( )
|
|
|
|
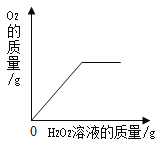
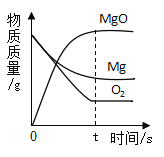
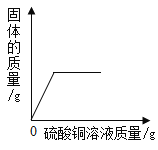
A.向一定质量的二氧化 锰中加入过氧化氢溶液 | B. 向等 质量的镁 粉和 铝粉中分别加入等浓度 的稀盐酸 | C. 镁在氧气中燃烧 | D. 向一定量铁粉和铜粉混 合物中加入硫酸铜溶液 |
A.AB.BC.CD.D