题目内容
【题目】二甲醚是一种应用前景广阔的清洁燃料.完全燃烧二甲醚4.6g,生成C028.8g,H2O 5.4g,下列判断不正确的是( )
A.二甲醚由C、H两种元素组成 B.二甲醚中C、H元素的质量比为4:1
C.二甲醚中H的质量分数为13% D.4.6g二甲醚完全燃烧消耗O29.6g
【答案】A
【解析】
试题分析:由题意,完全燃烧二甲醚4.6g,生成C028.8g,H2O 5.4g,8.8gC02中含碳元素的质量为8.8g×![]() 100%=2.4g,H2O5.4g中含氢元素的质量为5.4g×
100%=2.4g,H2O5.4g中含氢元素的质量为5.4g×![]() 100%=0.6g.
100%=0.6g.
A、由质量守恒定律,反应前后,元素种类、质量不变,二甲醚中C、H元素的质量之和为2.4g+0.6g=3g<4.6g,则二甲醚中一定含有氧元素,故选项说法错误.
B、由质量守恒定律,反应前后,元素种类、质量不变,二甲醚中C、H元素的质量分别为2.4g、0.6g,则二甲醚中C、H元素的质量比为2.4g:0.6g=4:1,故选项说法正确.
C、二甲醚中H的质量分数为![]() 100%≈13%,故选项说法正确.
100%≈13%,故选项说法正确.
D、由质量守恒定律,4.6g二甲醚完全燃烧消耗O2的质量为8.8g+5.4g﹣4.6g=9.6g,故选项说法正确.
故选A.

 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案【题目】某化学兴趣小组发现将足量的铜片与浓硫酸混合加热,可以产生气体并闻到刺激性气味,反应停止后,所得溶液呈蓝色。同学们对产生的气体和所得溶液的成分产生了兴趣,进行了下列实验探究。
【探究活动1】产生的气体是什么?
【提出猜想】猜想一:SO2;猜想二: SO2和H2。你认为猜想______ 是错误的。
【查阅资料】(1) S02是一种无色,有刺激性气味,有毒的气体。(2)S02可使品红溶液的
红色褪去。(3) S02与C02有相似的化学性质。
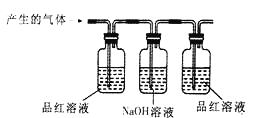
【实验验证】小明用如下图所示的装置进行实验,观察到____________;证明该气体是二氧化硫,该装置中氢氧化钠溶液的作用__________________。
【探究活动2】蓝色溶液的溶质是什么?
【提出猜想】猜想一:CuS04;猜想二:CuS04和H2S04.
【进行实验】取一定量反应后的溶液进行稀释,并分装在A、B两支试管中,然后进行下列实验,并完成如表:
步骤 | 实验操作 | 实验现象 | 实验结论 |
步骤一 | 在试管A中加入少量的CuO粉末 | 黑色粉末逐渐溶解 | 溶液中含有H2SO4 o4 |
步骤二 | 在试管B中加入过量的NaOH溶液 | _____________。 | 溶液中含有CuS04 |
【结论】通过实验,猜想二正确。
【拓展与反思】(1)根据以上探究活动,请写出铜与浓硫酸发生反应的化学方程式__________。
(2)小华同学经过认真思考后认为:在“探究活动2”的实验中,步骤一是多余的,足量的铜片与浓硫酸的反应停止后,所得溶液中一定含H2S04,理由是____________________。