题目内容
【题目】配平下列化学方程式(化学计量数为1也要填入“ ”内)
(1)________Fe+________Cl2![]() ________FeCl3
________FeCl3
(2)______WO3+______H2 ![]() _____W+_____H2O
_____W+_____H2O
(3)_______C2H5OH+______O2![]() ______CO2+______H2O
______CO2+______H2O
(4)_______Fe2O3+_______CO ![]() _____Fe+_______CO2
_____Fe+_______CO2
(5)________FeS2+_______O2![]() _______Fe2O3+_______SO2
_______Fe2O3+_______SO2
(6)________Al +________ Fe3O4![]() ________Fe +________ Al2O3
________Fe +________ Al2O3
(7)_______Fe(OH)3 +_______H2SO4 ═ _______Fe2(SO4)3+ _______ H2O
【答案】 2 3 2 1 3 1 3 1 3 2 3 1 3 1 3 4 11 2 8 8 3 9 4 2 3 1 6
【解析】根据配平方法可以配得下列方程式为;
(1)2Fe+3Cl2![]() 2FeCl3
2FeCl3
(2)WO3+3H2 ![]() W+3H2O
W+3H2O
(3)C2H5OH+3O2![]() 2CO2+3H2O
2CO2+3H2O
(4)Fe2O3+3CO ![]() 2Fe+3CO2
2Fe+3CO2
(5)4FeS2+11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
(6)8Al +3Fe3O4![]() 89Fe +4Al2O3
89Fe +4Al2O3
(7)2Fe(OH)3 +3H2SO4 ═Fe2(SO4)3+6 H2O

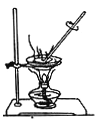
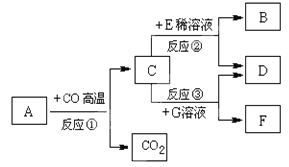
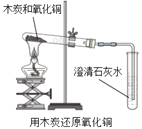
【题目】某化学兴趣小组用下图所示装置完成木炭还原氧化铜的实验,并对生成的红色固体成分进行探究。
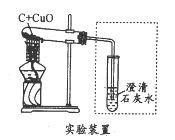
【提出问题】木炭与氧化铜反应生成的红色固体中含有什么物质?
【查阅资料】木炭与氧化铜反应也可能生成氧化亚铜(Cu2O);氧化亚铜是红色固体,能与稀硫酸反应: ![]() 。
。
【进行猜想】木炭与氧化铜反应生成的红色固体成分:
全部是铜;②全部是氧化亚铜;③是两者的混合物。
【实验探究】(1)用上图所示装置完成木炭还原氧化铜的实验,观察到澄清石灰水_______。试管冷却后,观察到黑色固体全部变为红色,对生成的红色固体成分进行探究:
实验探究
步骤 | 现象 | 结论 |
①取1.8g红色固体于试管中,滴加足量___________ ,充分反应 | ___________ | 猜想①错误 |
②过滤,将滤渣洗涤、干燥、称量 | 所得固体质量大于_______________ 克 | 猜想③正确 |
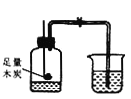
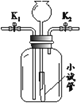
【题目】某化学兴趣小组利用下图装置进行实验。实验前K1、K2 均已关闭。
实验装置 | 【实验1】制取O2 | 【实验2】用NaOH溶液除去 O2中混有的CO2 |
| I.广口瓶中放入少量MnO2 II.打开K2,从长颈漏斗加入H2O2溶液至溢出小试管 | I.打开K1、K2,从长颈漏斗加入足量NaOH溶液至瓶中液面高于左侧导管口且低于小试管口 II. …… |
(1)连接仪器后,加水至长颈漏斗中形成液柱。一段时间后,液面高度保持不变,该现象说明______。
(2)实验1:制取O2的化学方程式是______。
(3)实验2:
①II中操作是:从______(填“左”或“右”)侧导气管通入混合气体。
②除去CO2 的反应如下,补全该反应的化学方程式:2NaOH + CO2 === Na2CO3 + ______
③实验过程中,当通入气体的流速突然变大时,小试管可以防止广口瓶中大量液体从长颈漏斗上口溢出,其原因是______。
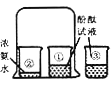
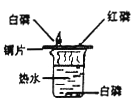
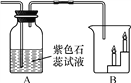
【题目】对比、归纳是化学学习的重要方法,请补充完成下列实验报告。
【实验目的】探究物理变化和化学变化
【实验过程】
实验操作 | 实验现象、分析或结论 | |
实验一 | 步骤一:取少量硫酸铜晶体放在研钵内观察。 | 现象:晶体为蓝色 |
步骤二:用研杵将硫酸铜晶体研碎 | 现象:___________________。 | |
步骤三:在2支试管中分别放入少量研碎前、后的硫酸铜晶体,并进入少量水,振荡得到澄清的硫酸铜溶液 | 现象:研碎后的硫酸铜晶体溶解的更快。 分析:原因是_______________________。 | |
步骤四:向上述两支试管中各滴加少量氢氧化钠溶液 | 现象:2支试管中均有蓝色不溶物生成。 分析: (1)该反应的化学方程式是_________; (2)该对比实验得出的实验结论是_______。 | |
实验二 |
| 现象:有部分黑色粉末变红,澄清石灰水变浑浊。 分析: (1)粉末由黑色变成红色的过程中发生化学反应的化学方程式是___________; (2)上述现象说明木炭和氧化铜发生了化学变化。 |
【实验结论】有他物质生成的变化叫化学变化,没有其他物质生成的变化叫物理变化。