题目内容
【题目】(10分)天然水净化为自来水的主要流程如下:
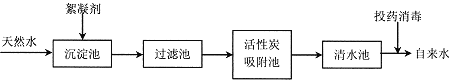
(1)下列说法不正确的是(填字母) 。
A.过滤池可以除去难溶性杂质
B.活性炭吸附池可以除去水中的色素和臭味
C.清水池中一定是软水
(2)明矾[KAl(SO4)m·12H2O]能作絮凝剂,是因为明矾溶于水后生成具有吸附作用的胶状物氢氧化铝。m= ,氢氧化铝的化学式为 。
(3)目前不少自来水用液氯(Cl2)作为消毒剂,液氯注入水后发生反应的示意图:
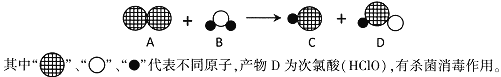
①C物质的水溶液能使紫色的石蕊溶液变成 色。取C物质的水溶液少许,向其中加入稀硝酸和硝酸银溶液,观察到有白色沉淀产生,发生反应的化学方程式是 ,利用此法可检验自来水中是否含有Cl—。
②液氯与水反应的化学方程式是 。
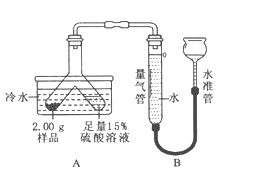
(4)天然水中微生物使有机物(以C6H10O5表示)转化为CO2和H2O的过程中所需O2的量叫做生化需氧量(BOD,单位为mg/L)。反应的化学方程式为:C6H10O5+6O2
【答案】(1)C (2)2 Al(OH)3 (3)①红 HCl+AgNO3==AgCl↓+HNO3
②Cl2+H2O=HCl+HClO (4)12.5mg/L
【解析】
试题分析:(1)A、过滤池可以除去难溶性杂质,正确,B、活性炭具有吸附性,故活性炭吸附池可以除去水中的色素和臭味,正确,C、清水池中的水只是除去了难溶性杂质以及颜色、异味,并没有除去可溶性的钙镁化合物,故不一定是软水,错误
(2)根据元素化合价的一般规律:在化合物中,正负化合价的代数和为0,在[KAl(SO4)m·12H2O]中K的化合价为+1,Al的化合价为+3,SO4的化合价为-2,故m=2;氢氧化铝的化学式为:Al(OH)3
(3)①根据微粒示意图,物质C为氯化氢,其水溶液为盐酸,故能使紫色的石蕊溶液变成红;向其中加入稀硝酸和硝酸银溶液,观察到有白色沉淀产生,发生反应的化学方程式是:HCl+AgNO3==AgCl↓+HNO3
②根据反应微粒示意图,液氯与水反应的化学方程式是Cl2+H2O=HCl+HClO
(4)根据化学方程式:C6H10O5+6O2
解:设氧气的质量为x
C6H10O5+6O2
162 192
10.8mg x
162:192=10.8mg:x
x=12.8mg
该水样的BOD的值=12.8mg÷1L=12.8mg/L