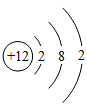题目内容
【题目】研究性学习小组选择“过氧化氢分解生成氧气的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程。
(提出猜想)过氧化氢分解生成氧气的快慢与催化剂的种类有关。
(实验方案)常温下,取两份体积相同、浓度相同的过氧化氢溶液,分解加入二氧化锰和红砖粉末,测定各收集一瓶(体积相同)氧气所需要的时间。
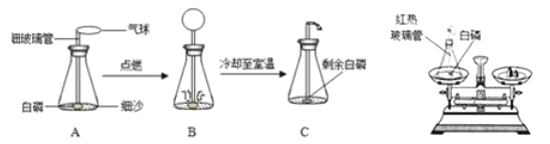
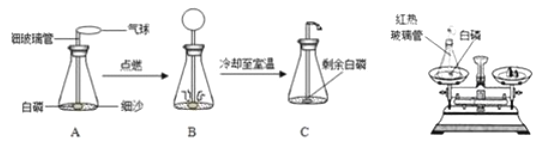
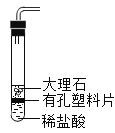
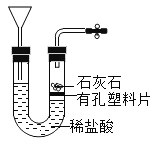
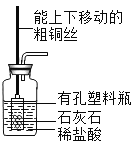
(进行实验)实验装置如图所示,组装好实验装置后,首先要_______________,再将分液漏斗中的液体加入锥形瓶中,立即收集一瓶气体,此实验中宜采用的收集气体的方法是____________。
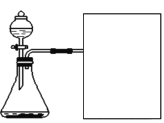
(实验记录)
试验编号 | ① | ② |
反应物 | 5%过氧化氢溶液50g | 5%过氧化氢溶液50g |
催化剂 | 红砖粉末 | 1g二氧化锰 |
收集气体所需时间 | 165s | 46s |
实验①中加入红砖粉末的质量是__________ g。
(得出结论)该探究过程得出的结论是____________________。
(反思)过氧化氢在常温下分解缓慢,加入二氧化锰或红砖粉末后分解速率明显加快,若要证明二氧化锰和红砖粉末是否为该反应的催化剂,还需要增加实验来验证它们在化学反应前后的 __________和________是否改变。
【答案】检查装置的气密性 排水法 1 相同条件下,过氧化氢分解生成氧气的快慢与催化剂的种类有关 质量 化学性质
【解析】
进行实验:
实验装置如图所示,组装好实验装置后,首先要检查装置的气密性;氧气不易溶于水,且密度比空气大,因此可以采用排水法或向上排空气法收集,因为需要观察收集一瓶气体所用的时间,用排水法更好一些;
实验记录:
根据控制变量法,分析表中的有关数据,可知分别用1g红砖粉和1gMnO2做催化剂,来催化反应时所用的时间分别是165s和46s;由此可知,用1gMnO2做催化剂要比用1g红砖粉做催化剂时,化学反应速率要快。
得出结论:
由实验现象可知,相同条件下,H2O2生成O2的快慢与催化剂的种类有关;
反思:
根据催化剂的概念可知,催化剂能改变化学反应的速率,而本身的质量和化学性质在反应前后不改变。

【题目】常用仪器的使用、常见气体的制取是初中化学实验的基础内容。如图是实验室常用的仪器,请回答下列问题:
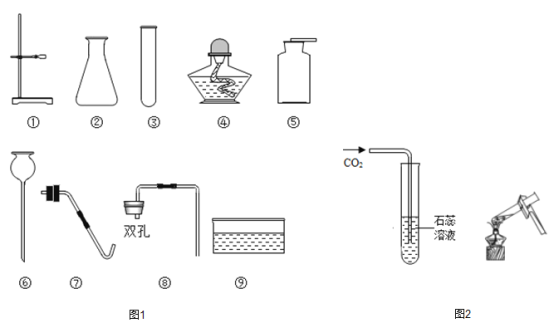
(1)写出图1中标号④的仪器名称_____________。
(2)若要组装一套用高锰酸钾制取并收集氧气的装置,可选择的仪器组合为_________(填序号),该装置中还需要的种实验用品是_________,发生反应的化学方程式为__________,实验中有些错误操作可能会使试管炸裂,写出为避免试管炸裂的一个操作___________。
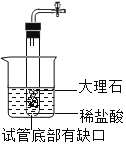
(3)实验室制取二氧化碳选用的药品是___________(填名称),一般不用排水法收集二氧化碳的原因是_______。实验结束后,小静发现试管内仍有固体剩余,她处理的办法是_______________。
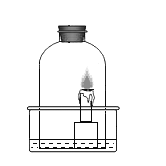
(4)某同学利用如图2装置进行二氧化碳的性质探究实验时,将制得的二氧化碳通入紫色石蕊溶液中,溶液变红,但将变红的溶液加热时,溶液没有变紫色。于是小组同学对产生该现象的原因进行了下列探究。
(提出猜想)猜想①:紫色石蕊溶液已变质;猜想②:二氧化碳中混有较多氯化氢。
同学们经过讨论后很快就排除了猜想①,其原因是_________。
(设计实验)请设计实验验证猜想②正确。
实验操作 | 实验现象 |
_______ | _______ |
(5)实验室可以用草酸脱水的方法来制取氧化碳,反应原理如下: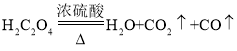 ,为获得较纯净的一氧化碳,可采取___________方法净化。
,为获得较纯净的一氧化碳,可采取___________方法净化。