题目内容
【题目】元素周期表是学习和研究化学的重要工具,它的内容十分丰富。下表是元素周期表的部分内容,请认真分析并回答后面的问题;
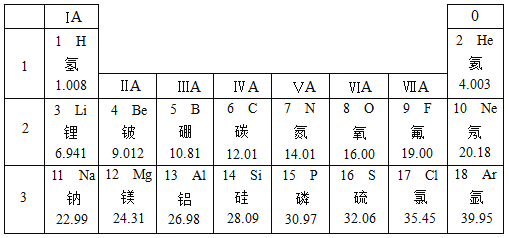
(1)表中磷原子的核电荷数为___________,铝原子的电子数为___________。
(2)表中具有相对稳定结构的元素是_____________。
(3)从上表中查出地壳中含量最多的金属元素的相对原子质量为________。
(4)表中不同元素最本质的区别是____________(填序号)。
A 相对原子质量不同 B 质子数不同 C 中子数不同
(5)1869年,___________(填字母)发现了元素周期律并编制出元素周期表。
A 张青莲 B 门捷列夫 C 拉瓦锡
(6)元素周期表中,原子序数为12的镁元素的原子结构示意图如下图所示,该原子在化学反应中易___________(选填“得到”或“失去”)电子。说明元素的化学性质与原子的___________关系密切。
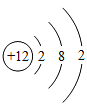
(7)元素周期表中每一个横行叫作一个周期,通过分析,同一周期元素之间的排列有一定的规律,例如:
①从左到右,由金属元素逐渐向非金属元素过渡;
②__________;
③_______________。
【答案】15 13 氦、氖、氩 26.98 B B 失去 最外层电子数 从左向右,元素的原子序数依次递增 从左向右,相邻元素的原子序数相差1(只要合理均可)
【解析】
(1)磷元素为第15号元素,磷原子的核电荷数=原子序数=15,铝元素为13号元素,铝原子的电子数=原子序数=13.
(2)原子只有一个电子层时,最外层电子数是2,属于稳定结构,但电子层数大于1层时2,原子最外电电子数是8,属于稳定结构,具有相对稳定结构的元素是:氦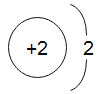 、氖
、氖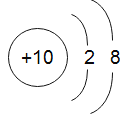 、氩
、氩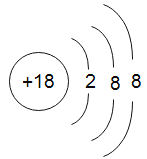 ;
;
(3)地壳中含量最多的金属元素是铝元素,其相对原子质量为:26.98;
(4)表中不同元素最本质的区别是:质子数(或核电荷数)不同;
故选:B。
(5)1869年,门捷列夫发现了元素周期律并编制出元素周期表。
A 张青莲,测定部分元素的相对原子质量;
B 门捷列夫,发现了元素周期律并编制出元素周期表;
C 拉瓦锡,测定空气中氧气含量;
故选:B。
(6)元素周期表中,原子序数为12的镁元素的原子最外层有2个电子,(小于4)该原子在化学反应中易失去2个电子。说明镁元素的化学性质与原子的最外层电子数关系密切。
(7)元素周期表中每一个横行叫作一个周期,通过分析,同一周期元素之间的排列有一定的规律,例如:
①从左到右,由金属元素逐渐向非金属元素过渡;
②从左向右,元素的原子序数依次递增;
③从左向右,相邻元素的原子序数相差1。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】研究性学习小组选择“过氧化氢分解生成氧气的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程。
(提出猜想)过氧化氢分解生成氧气的快慢与催化剂的种类有关。
(实验方案)常温下,取两份体积相同、浓度相同的过氧化氢溶液,分解加入二氧化锰和红砖粉末,测定各收集一瓶(体积相同)氧气所需要的时间。
(进行实验)实验装置如图所示,组装好实验装置后,首先要_______________,再将分液漏斗中的液体加入锥形瓶中,立即收集一瓶气体,此实验中宜采用的收集气体的方法是____________。
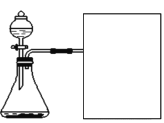
(实验记录)
试验编号 | ① | ② |
反应物 | 5%过氧化氢溶液50g | 5%过氧化氢溶液50g |
催化剂 | 红砖粉末 | 1g二氧化锰 |
收集气体所需时间 | 165s | 46s |
实验①中加入红砖粉末的质量是__________ g。
(得出结论)该探究过程得出的结论是____________________。
(反思)过氧化氢在常温下分解缓慢,加入二氧化锰或红砖粉末后分解速率明显加快,若要证明二氧化锰和红砖粉末是否为该反应的催化剂,还需要增加实验来验证它们在化学反应前后的 __________和________是否改变。