题目内容
【题目】控制变量法是实验探究的重要方法。下列四组对比实验获得的结论正确的是
选项 | 实验操作 | 结论 |
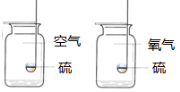
A | | 呼出的气体全部都是CO2 |
B | | O2含量越高,反应越剧烈 |
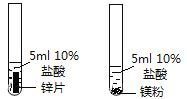
C | | 铁生锈一定有O2参与 |
D | | 镁的活动性比锌强 |
【答案】B
【解析】
试题分析:A、根据呼出的气体使澄清石灰水变得更浑浊,可得出呼出的气体比空气含较多CO2,并不能说明全部都是CO2,错误,B、根据硫在氧气中燃烧比在空气中燃烧更激烈,可得出O2含量越高,反应越剧烈,正确,C、设计探究性实验时,要注意控制变量,2个试管中不同的是前者有水,后者没有水,所以得出铁生锈一定有水参与,错误,D、设计探究性实验时,要注意控制变量,一个是锌片,一个是镁粉,反应物的接触面积不同,所以无法比较,错误,故选B

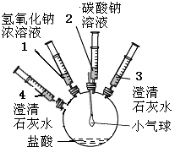
【题目】(11分)某实验小组的同学要探究酸碱盐中碳酸钠的化学性质,设计了如下实验装置及方案:
实验装置 | 实验步骤及操作 | 实验现象 |
| ①将注射器2中的溶液推入盛有稀盐酸的瓶中,至不再有气泡产生。 | 气球变瘪 |
②将注射器3稍稍向外拉 | 澄清石灰水变浑浊 | |
③将注射器1中的溶液推入瓶中 | 气球鼓起 | |
④ | 无明显现象 | |
⑤将注射器4中的溶液推入瓶中 |
(一)(1)步骤①中气球变瘪的原因 ;
(2)步骤①、②可得出碳酸钠具有 的性质;
(3)步骤④的操作是 ,其目的是 ;
(4)步骤⑤中发生反应的化学方程式 ;
(5)步骤③④⑤可得出碳酸钠具有 的性质;
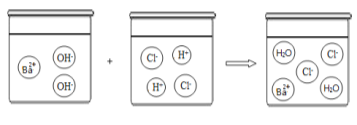
(二)上述实验结束后,实验小组的同学又对瓶内溶液的成分十分好奇,进行了探究:
(1)【提出猜想】通过分析,一致认为瓶内溶液的溶质中一定含有 ,可能含有氢氧化钙或 。
(2)【实验验证】设计实验方案确定溶液中溶质的组成.
实验操作 | 实验现象 | 实验结论 |
分别取少量溶液于A、B两支试管中,A中 加入CaCl2溶液,B中加入Na2CO3溶液 | A中产生白色沉淀,B中没有沉淀 | 瓶内溶液中溶质的成分为 |
(3)【反思与交流】根据所学化学知识,除了以上方案外,下列哪些物质可以代替试管B中加入的Na2CO3溶液完成该实验? (填序号)
a.K2CO3 b.BaCO3 c.CO2 d.无色酚酞 e. CuSO4