题目内容
【题目】(8分)
(1)下列关于氢氧化钡性质的描述中,属于碱的共同性质的是
A.能使紫色石蕊溶液变蓝色 B.能与盐酸反应生成水
C.能与Na2SO4溶液反应生成BaSO4沉淀 D.能与CO2反应生成水
(2) 氢氧化钡与其它不同的碱表现出一些共同的性质,这是因为碱溶液中都含有 (用符号表示)。
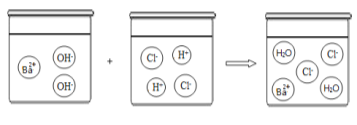
(3)根据下图可以看出酸与碱发生中和反应的微观本质是 。
(4)请写出氢氧化钡与下列物质反应的化学方程式:
①与CO2反应: ;
②与CuCl2溶液反应: 。
【答案】(1)B (2)Ba2+ (3)OH-+H+== H2O
(4)①CO2 +Ba(OH)2 ==BaCO3↓+ H20 ②Ba(OH)2+CuCl2==BaCl2+Cu(OH)2↓
【解析】
试题分析:(1)A、碱溶液能使紫色石蕊溶液变蓝色,如果是不溶性碱,就不能在溶液中电离出OH-,也就不能能使紫色石蕊溶液变蓝色,错误,B、能与盐酸反应生成水,正确,C、能与Na2SO4溶液反应生成BaSO4沉淀,只是Ba(OH)2的化学性质,错误,D、可溶性碱能与CO2反应生成水,而不溶性碱不能,错误,故选B
(2)碱表现出一些共同的性质:是因为碱溶液中都含有OH-,氢氧化钡与其它不同的碱表现出一些共同的性质,这是因为碱溶液中都含有Ba2+
(3)酸与碱发生中和反应的微观本质是:OH-+H+== H2O
(4)①氢氧化钡与CO2反应化学方程式:CO2 +Ba(OH)2 ==BaCO3↓+ H20
②氢氧化钡与CuCl2溶液反应化学方程式:Ba(OH)2+CuCl2==BaCl2+Cu(OH)2↓

 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案【题目】(7分)四氧化三铁可用于医疗器械、电子等工业。某实验兴趣小组从工厂采集废液(含FeSO4和少量ZnSO4、MgSO4),进行四氧化三铁的制备实验。
【阅读资料】
(1)25℃时,氢氧化物沉淀的pH范围如表所示。
Zn(OH)2 | Fe(OH)2 | Mg(OH)2 | |
开始沉淀的pH | 5.7 | 7.6 | 10.4 |
沉淀完全的pH | 8.0 | 9.6 | 12.4 |
(2)25℃时,Zn(OH)2可溶于pH>10.5的碱溶液。
(3)制备Fe3O4的实验流程如下:
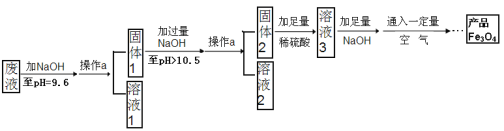
【回答问题】
(1)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为 (写出其中一个)。
(2)操作a的名称为 。该操作需要的玻璃仪器有烧杯、玻璃棒、 等。玻璃棒在此操作中的主要作用是 。
(3)溶液1所含溶质有 (至少写两种成分的化学式);溶液3所含溶质的主要成分为 (写名称)。