题目内容
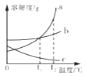
【题目】向盛有饱和澄清石灰水的烧杯中持续通入CO2出现了异常现象(先变浑浊后又变澄清.提示:过量的CO2会与CaCO3等反应生成可溶于水的Ca(HCO3)2),兴趣小组同学利用数字分析仪进行研究,测定记录得到溶液的导电性变化随二氧化碳的质量关系如下图所示.下列说法不正确的是( ) 
A.ab段溶液逐渐变浑浊,bd段溶液逐渐变澄清
B.b点溶液溶液碱性最强
C.bd段反应为:CaCO3+CO2+H2O═Ca(HCO3)2
D.c点溶液中含有2种溶质,沉淀质量为15g
【答案】BD
【解析】解:ab段溶液的导电性逐渐减小到零,说明是氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,bd段溶液的导电性逐渐增大,说明是碳酸钙和水、二氧化碳反应生成溶于水的碳酸氢钙,所以 A、ab段溶液逐渐变浑浊,bd段溶液逐渐变澄清,故A正确;
B、b点的溶液显中性,故B错误;
C、bd段溶液的导电性逐渐增大,说明是碳酸钙和水、二氧化碳反应生成溶于水的碳酸氢钙,化学方程式为:CaCO3+CO2+H2O═Ca(HCO3)2 , 故C正确;
D、c点的溶液中含有碳酸氢钙一种溶质,
4.4g二氧化碳生成的碳酸钙沉淀质量为x
CO2﹣﹣﹣ | CaCO3 |
44 | 100 |
4.4g | x |
![]() =
= ![]()
x=10g,
二氧化碳和水反应掉的碳酸钙质量为y
CO2﹣﹣﹣ | CaCO3 |
44 | 100 |
2.2g | y |
![]() =
= ![]()
y=5g
所以沉淀质量为5g,故D错误.
故选:BD.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目