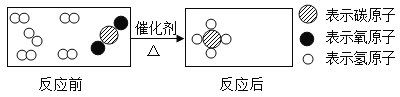
题目内容
【题目】实验是实现科学探究的重要途径,请回答下列有关化学实验的问题。
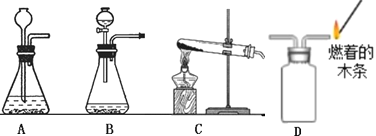
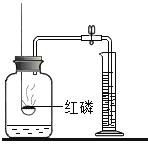
(1)利用B装置制取一种气体,写出有关反应的化学方程式____________。
(2)实验室可用氯化钠固体和浓硫酸在加热条件下反应制取氯化氢气体,该气体极易溶于水,则制取氯化氢应选择的发生装置和收集装置分别为_____________(填字母),请写出一种方法验证收集到的气体。_________
【答案】2KClO3![]() 2KCl + 3O2 ↑ AF 将生成气体通入硝酸银溶液,若产生白色沉淀,则收集到的气体是氯化氢
2KCl + 3O2 ↑ AF 将生成气体通入硝酸银溶液,若产生白色沉淀,则收集到的气体是氯化氢
【解析】
(1)利用B装置制取一种气体,B装置是固体加热型,可用氯酸钾与二氧化锰混合物加热制取氧气,氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,反应的化学方程式为:2KClO3![]() 2KCl + 3O2 ↑;
2KCl + 3O2 ↑;
(2)根据“实验室可用氯化钠固体和浓硫酸在加热条件下反应制取氯化氢气体”,可知该反应物是固体与液体,反应的条件是加热,选择的发生装置是A;根据“该气体极易溶于水”可知,不能用排水法收集,氯化氢密度大于空气,可用向上排空气法收集,选择的收集装置是F;氯化氢溶于水形成盐酸,盐酸能与硝酸银反应生成氯化银沉淀和硝酸,验证收集到的气体方法是将生成气体通入硝酸银溶液,若产生白色沉淀,则收集到的气体是氯化氢。

 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案【题目】小明同学为了测定市面销售的某品牌纯碱中碳酸钠的质量分数(杂质为氯化钠,氯化钠溶于水且不与氯化钙反应),进行了如下实验:①在三个烧杯中分别加入11.0g 样品及足量的水配成溶液;②向三个烧杯中分别加入一定质量的10.0%的氯化钙溶液;③将充分反应后生成的沉淀过滤、洗涤、干燥,并称量得到的白色固体。实验所得数据见下表,请你分析并进行有关计算:
烧杯Ⅰ | 烧杯Ⅱ | 烧杯Ⅲ | |
加入10.0%氯化钙溶液的质量/g | 55.5 | 120.0 | 150.0 |
白色固体的质量/g | 5.0 | 10.0 | 10.0 |
(1)在图中绘制出白色沉淀与加入氯化钙溶液的质量关系图(图上要注明白色沉淀、氯化钙溶液的相关质量)。______
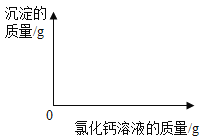
(2)样品中碳酸钠的质量分数是_____?(结果精确到0.1%)
(3)烧杯Ⅱ所得溶液中氯化钠的溶质质量分数是_______?(结果精确到0.1%)
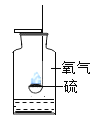
【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
A | B | C | D | |
实验装置 |
硫在氧气中燃烧 |
测定空气中氧气含量 |
铁丝在氧气中燃烧 |
排水法收集氢气 |
解释 | 集气瓶中的水:吸收放出的热 | 量简中的水:通过水体积的变化得出O2体积 | 集气瓶中的水:冷却溅落融熔物,防止集气瓶炸裂 | 集气瓶中的水:先将集气瓶内的空气排净,后便于观察H2何时收集满 |
A.AB.BC.CD.D