题目内容
【题目】CO2 的资源化利用日趋成为研究热点。某化学兴趣小组查阅资料发现:CO2 与 H2 能在催化剂表面反应生成 CH4与H2O;CH4与CuO在高温下反应能得到多种产物。为探究上述反应,设计如下装置:
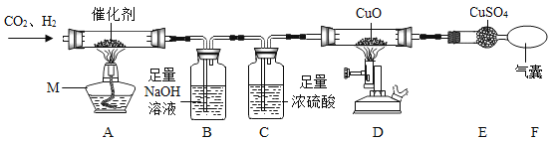
反应一段时间后,兴趣小组同学发现D中固体由黑色变成紫红色,E中固体由白色变为蓝色(CuSO4·5H2O)。
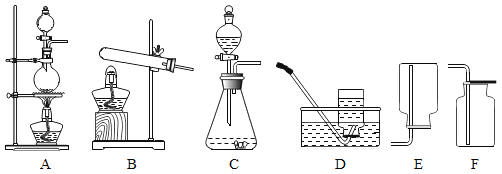
(1)M的名称为_____;装置C的作用是_____。
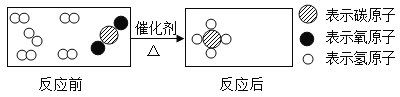
(2)CO2与H2的反应可用下图表示。请在“反应后”的方框内画出除![]() 外所有分子的模型_____。
外所有分子的模型_____。
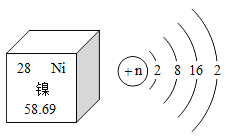
(3)①上述反应常使用镍(Ni)作催化剂。已知镍元素在周期表中的相关信息及镍原子结构示意图如图所示,则n=_____。
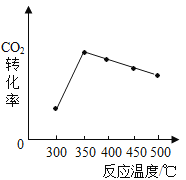
②CO2与H2的反应过程中,反应温度对CO2转化率的影响如图所示。实验时,应控制的最佳反应温度是_____℃。
(4)将气囊中的气体通入澄清的石灰水,发现溶液变浑浊。试综合以上信息,写出CH4与CuO在高温下反应的化学方程式:_____。
(5)实验过程中,B中NaOH溶液共吸收了2.2g CO2气体。请通过计算确定此时溶液中生成的Na2CO3的质量_____。
【答案】酒精灯 干燥气体或吸收气体中的水蒸气 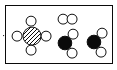 28 350
28 350 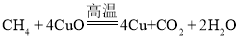 5.3g
5.3g
【解析】
二氧化碳和氢气在催化剂和加热条件下反应生成甲烷和水蒸气,经过B和C装置,吸收剩余的二氧化碳和水蒸气后,甲烷和氧化铜在高温下反应,D中固体由黑色变成紫红色,即由氧化铜变成了铜,E中固体由白色变为蓝色(CuSO4·5H2O),说明有水生成,将气囊中的气体通入澄清的石灰水,发现溶液变浑浊,说明有二氧化碳生成,则该反应的产物为铜、水和二氧化碳,化学方程式为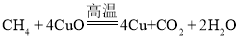 。
。
(1)装置A中仪器M的名称是酒精灯;装置C中盛放的是浓硫酸,浓硫酸具有吸水性,因此该装置作用是干燥气体或吸收气体中的水蒸气。
(2)根据题意,二氧化碳和氢气在催化剂和加热条件下反应生成甲烷和水蒸气,化学方程式为: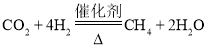 ,根据化学方程式可知反应后有1个甲烷分子,2个水分子和一个氢气分子,故图示为:
,根据化学方程式可知反应后有1个甲烷分子,2个水分子和一个氢气分子,故图示为: 。
。
(3)根据镍元素信息示意图或镍原子结构示意图可知,Ni为28号元素,所以Ni的核电荷数为28。根据图像可知,当反应温度为350℃时,二氧化碳的转化率最高,生成的甲烷最多,所以最佳反应温度为350℃。
(4)根据分析可知,CH4与CuO在高温下反应生成铜、水和二氧化碳,化学方程式为: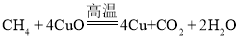 。
。
(5)解:设生成的Na2CO3的质量为x 。
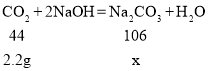
![]()
![]()
答:生成的Na2CO3质量为5.3g。

【题目】将一定量的乙醇(C2H5OH)和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水蒸气和一种未知物X.测得反应前后物质的质量如表.下列判断正确的是( )
物 质 | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
反应前质量/g | 4.6 | 8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 4.4 | 5.4 | m |
A.表中m的值为2.8
B.X可能是该反应的催化剂
C.该反应分解反应
D.物质X一定含有碳元素,可能含有氢元素