题目内容
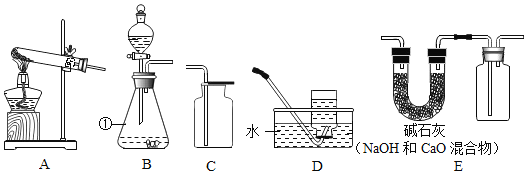
【题目】在实验室利用下列仪器进行制取气体的实验。请回答下列问题:
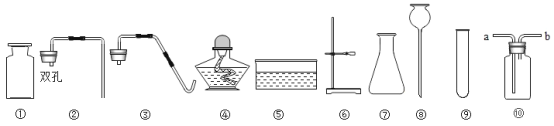
(1)写出图中仪器⑤的名称:_________。
(2)实验室用氯酸钾制取并收集氧气,反应的化学方程式为________ 。需要选择图 1 中的仪器有________(填序号)。
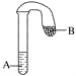
(3)常温下,用锌和稀硫酸反应制取氢气,反应的化学方程式为________; 若用装置⑩收集氢气,气体应从______(填“a”或“b”)端导管进入。要想获得干燥的氢气,可将气体通过装有____________(填试剂名称)的洗气瓶。
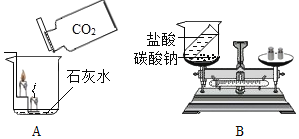
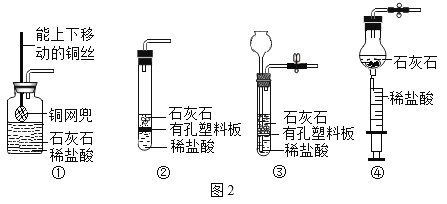
(4)图2为制备二氧化碳的发生装置,其中不能控制“反应随时发生与停止”的是_____________(填序号),原因是____________。
【答案】水槽  ①③④⑤⑥⑨
①③④⑤⑥⑨ ![]() b 浓硫酸 ② 不能实现固体与液体的分离
b 浓硫酸 ② 不能实现固体与液体的分离
【解析】
(1)据图可知仪器⑤的名称是水槽;
(2)加热氯酸钾和二氧化锰生成氯化钾和氧气,反应的化学方程式为 ;该反应需要加热,氧气的密度比空气大,不易溶于水,可用排水法或向上排空气法收集,所以需要选择上图中的仪器有:①③④⑤⑥⑨;
;该反应需要加热,氧气的密度比空气大,不易溶于水,可用排水法或向上排空气法收集,所以需要选择上图中的仪器有:①③④⑤⑥⑨;
(3)锌和稀硫酸反应制取氢气,反应的化学方程式为![]() ;氢气的密度比空气小,若用装置⑩收集氢气,气体应从b端导管进入;浓硫酸有吸水性,可以干燥氢气;
;氢气的密度比空气小,若用装置⑩收集氢气,气体应从b端导管进入;浓硫酸有吸水性,可以干燥氢气;
(4)要实现反应随时发生与停止,反应装置要能够实现固体与液体的分离。
①可以通过移动铜丝控制反应的发生与停止,不符合题意;
②不能实现固、液分离,不能控制反应的发生与停止,符合题意;
③可以通过右端弹簧夹的开与关来控制反应的发生与停止,不符合题意;
④可以通过注射器控制固、液分离,能控制反应的发生与停止,不符合题意。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】石灰石是我市主要矿产之一,小江同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验.
实验步骤 | ①称取烧杯的质量 | ②将适量盐酸加入烧杯中并称重 | ③称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 | ④待反应完全后,称重 |
实验图示 |
| |||
实验数据 | 烧杯的质量为50.0g | 烧杯和盐酸的质量为100.0g | 石灰石样品样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
试通过分析计算:
(1)该实验中生成的二氧化碳的质量是多少克?
(2)该石灰石样品的纯度是否符合要求?(假设石灰石样品中的杂质不与盐酸反应也不溶于水)