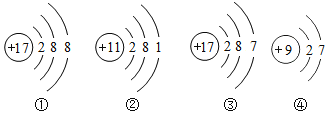
��Ŀ����
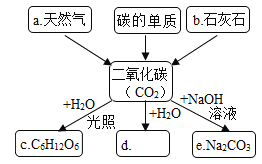
����Ŀ��ͼ��A��B��C��D��E�廷�ֱ�������л�ѧ�г������������ʣ�����������ʾ��������֮���ܷ�����ѧ��Ӧ������A��E�����¶��Ǻ�ɫ���壬��EΪһ�ַǽ������ʣ�B��C��D�����¾�Ϊ��ɫ���壬����BΪ������õIJ���֮һ��C�Ĺ���������˹����ꣻA��D��Ӧ������һ�ֺ�ɫ�����C��
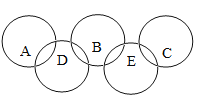
��1��д������A��E�Ļ�ѧʽΪ________ ��_______��
��2��ʵ���ҳ���___________���ѧʽ������C���壬��д���÷�Ӧ�Ļ�ѧ����ʽ��_______________��
���𰸡�CuO C Ca��OH��2 Ca��OH��2+CO2=CaCO3��+H2O
��������
B�ǹ�����õIJ���֮һ��Ϊ��ɫ���壬����BΪ��������C�Ĺ���������˹����꣬����CΪ������̼������A��E���Ǻ�ɫ���壬��E�Ƿǽ������ʣ��ڳ���ֻ��̼�Ǻ�ɫ�ķǽ������ʣ�����EΪ̼��A����Ϊ����ͭ���߶������̻�����������������AD�ܹ���Ӧ�õ���ɫ����Ͷ�����̼�����ɫ����Ӧ��Ϊͭ����AΪ����ͭ��D��������ɫ���壬�Ҷ�Ӧ�����ж�����̼������DΪһ����̼��������֤��������ȷ��
�ɷ�����֪��1��AΪ����ͭ��EΪ̼����Ӧ�Ļ�ѧʽ�ֱ�Ϊ�� CuO��C��
��2������C�Ƕ�����̼����ʵ���Ҽ��������̼ʹ�õ��dz����ʯ��ˮ��������Ϊ�������ƣ����ڸ�Ԫ����+2�ۣ���������-1�ۣ����Ի�ѧʽΪCa��OH��2����Ӧ�ķ�Ӧ����ʽΪCa��OH��2+CO2=CaCO3��+H2O��

 Сѧ�̲�ȫ��ϵ�д�
Сѧ�̲�ȫ��ϵ�д�����Ŀ���ڻ�ѧѧϰ�����У����dz�����Ҫͨ����ѧ̽������ʶ���ʣ��о����ʵĻ�ѧ�仯������һ���������ʵ��̽����
��̽�����Թ�������ֽ�Ϊ�о��������ʵ�飬̽��Ӱ�컯ѧ��Ӧ���ʵ����أ�
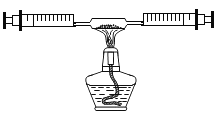
����С����ɲ�����ͼװ�ý���ʵ�飬��¼�ռ�10mL������ʱ�䣬ʵ���ҿɹ�ѡ����Լ��У�2.5%��5%��10%����Ũ�ȵ�H2O2��Һ��MnO2��CuO����ש��ĩ��
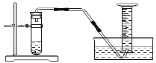
A�飺̽�������Ի�ѧ��Ӧ���ʵ�Ӱ��
ȡ5mL10%H2O2��Һ������ʵ��ֱ����0.5gMnO2����ש��ĩ��CuO����ʵ�飬��¼�������£�
�Լ� | MnO2 | ��ש��ĩ | CuO |
t/s | 10 | 60 | 20 |
�ɴ˿ɳ����ۣ�MnO2��CuO��H2O2�ֽ��д����ã���ש��ĩ�����ã�ijͬѧ�Ըý���������ʡ�
����Ա�ʵ�飬����Ϊ_____________________��
�������ʱ�䣨����100s�����ռ������������塣
�������ۣ���ש��ĩ�д����ã�������MnO2��Ч����ߡ�
B�飺̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ��
��ͬѧ��ȡ10mL5%H2O2��Һ������0.5gMnO2Ϊ����������ʵ�飬��¼ʱ��t1��
��ͬѧ��ȡ10mL2.5%H2O2��Һ������0.5g CuOΪ����������ʵ�飬��¼ʱ��t2��
ʵ����t1______t2����������������������
���ۣ�Ũ��Խ��Ӧ����Խ�졣
��ͬѧ����ʵ�����������ʣ�������ʵ��___________________��
��¼ʱ��t3����t1��t3��t2��
��������Ϊ�����������༰������ͬʱ����Ӧ��Ũ��Խ��____________��
C�飺̽��__________�Ի�ѧ��Ӧ���ʵ�Ӱ�졣
ȡ10mL5%H2O2��Һ��0.5gCuOΪ��������ʵ�飬����ʵ��ֱ��Թ����ڱ�ˮԡ��50����ˮԡ��¼ʱ��t4��t5����t4��t5��
���ۣ�����Ӧ��Ũ�Ⱥʹ�����ͬʱ��_____________________��
����������Ϊ���о�ijһ���ضԻ�ѧ��Ӧ���ʵ�Ӱ�죬����ֻ������һ��������������������ͬ��
��̽��������̼������̽����
��˿����̼��0.69%����������ȼ�գ���˿ȼ��ʱ�������䣬���о����������������������ԭ������ͬʱ������ij�����壬�Ʋ��������___________�������ƣ���
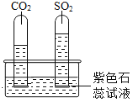
�������ϣ���CO2��SO2����ˮ��������ƵĻ�ѧ���ʢ����ǵ���ɫ����
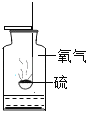
ʵ��һ��ˮ���е�����ɫʯ����ռ�������������Թ�ͬʱ���������У�Ƭ�̺�ʵ��������ͼ��ʾ��˵����ͬ�����µ��ܽ��ԣ�SO2_____��������������������CO2���Թ�����Һ���____________ɫ��
ʵ�������֪þ��������CO2�о���ȼ�գ���ӦΪ��Mg+CO2![]() MgO+C�����Ʋ�þ����SO2��ȼ�յ�����Ϊ������ȼ�ա��ų�����________________��
MgO+C�����Ʋ�þ����SO2��ȼ�յ�����Ϊ������ȼ�ա��ų�����________________��
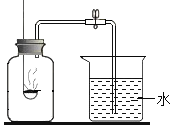
����Ŀ������ʵ��ָ�������е�ˮ�������û������ˮ����Ҫ���õ��ǣ�������
ѡ�� | A | B | C | D |
ʵ �� װ �� |
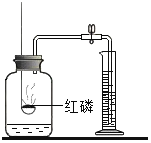
����������ȼ�� |
�ⶨ�������������� |
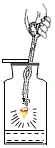
��˿��������ȼ�� |
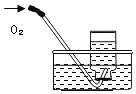
��ˮ���ռ����� |
���� | ����ƿ�е�ˮ�����շų������� | ��Ͳ�е�ˮ��ͨ��ˮ����ı仯�ó�O2��� | ����ƿ�е�ˮ����ȴ�����������ֹ����ƿը�� | ����ƿ�е�ˮ����ˮ������ƿ�ڵĿ����ž����ڹ۲�O2��ʱ�ռ��� |
A.AB.BC.CD.D
����Ŀ��ijУ��ѧ��ȤС������ʦָ���£������ˡ�Ӱ��˫��ˮ�ֽ����ء���ʵ�顣������̽��Ӱ�컯ѧ��Ӧ�������ص��������
ʵ����� | ����������ҺŨ��/% | ����������Һ����/g | �¶�/�� | ������������/g | �������/ml | ��Ӧ����ʱ��/s |
�� | 5 | 12 | 20 | 0.2 | 125 | 11 |
�� | 30 | 12 | 20 | 0.2 | 125 | 2 |
�� | 30 | 12 | 40 | / | 125 | 148 |
�� | 30 | 12 | 90 | / | 125 | 82 |
��1��ͨ��ʵ��ٺ͢ڶԱȿ�֪����ѧ��Ӧ������_________�йأ�
��2��ͨ���Ա�ʵ��_________��_________��֪����ѧ��Ӧ�������¶ȵĹ�ϵ�ǣ���ͬ�����£��¶�________����Ӧ����Խ�졣
��3��������ʵ���֪��ʵ�����ù���������ȡ����������ʵ������ǣ��¶�Ϊ_________��,���������Ũ��Ϊ_________% ����������_________����С����ޡ�����
��4��ʵ���г�����Ͳ�⣬����Ҫ�õ��IJ��������У�_________��
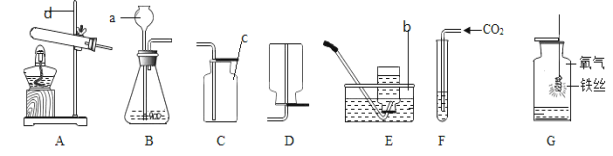
��5��Ϊ��ɱ�ʵ�飬�ռ�װ�ÿ���ѡ��ͼ�е� ____________������ţ�