题目内容
【题目】(12分)水是人类生活中不可缺少的物质。
(1)下列净水方法中,通常用于除去水中难溶性杂质的是_____,净水程度最高的是_____
A.过滤 B.煮沸 C.蒸馏 D.吸附
(2)自来水厂常用二氧化氯(ClO2)消毒,其中氯元素的化合价为________;
(3)自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一。请写出Ca(HCO3)2受热分解的化学方程式________________。
(4)为了探究水的组成,实验装置如图所示
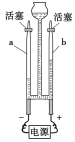
①该实验中,与两个电极相连的a、b两支玻璃管中产生的气体分别是 和 ,质量比为 。②写出该反应的化学方程式
(5)硬水给生活和生产带来很多麻烦,生活中常用 区分硬水和软水,常用 方法降低水的硬度。
【答案】(1)A;C;(2)+4;(3)Ca(HCO3)2![]() CaCO3↓+H2O+CO2↑;(4)氢气;氧气;1:8;2H2O
CaCO3↓+H2O+CO2↑;(4)氢气;氧气;1:8;2H2O![]() 2H2↑+O2↑;(5)肥皂水;煮沸;
2H2↑+O2↑;(5)肥皂水;煮沸;
【解析】
试题分析:(1)在水的净化中,过滤可以除去水中的难溶性固体物质,蒸馏可以除去水中的所有杂质故蒸馏的净化程度最高;(2)在化合物中,氧元素的化合价为-2,根据化合物中元素化合价的代数和为0可计算出氯元素的化合价为+4;(3)根据题目中提供的反应物、生成物、反应条件书写化学方程式;(4)在水的电解中,氢气和氧气的体积比为2:1,故可以根据气体的体积大小判断氢气和氧气;可以根据水中氢元素和氧元素的质量比计算生成的氢气和氧气的质量比;水在通电的条件下生成氢气和氧气,据此书写化学方程式;(5)硬水中含有的可溶性钙镁化合物比较多,硬水遇到肥皂水起的浮渣多,故可以用肥皂水来鉴别硬水和软水;硬水中含有的可溶性钙镁化合物在加热时可以形成不溶性的钙镁化合物,故可以采用煮沸的方法来降低水的硬度;