题目内容
【题目】某学校的探究性学习小组发现,铜绿[![]() ]受热分解后,除生成CO2和水蒸气外,试管中还有一些黑色粉末状固体。他们通过实验探究,分析黑色固体的组成,并验证产生的气体。请填空:
]受热分解后,除生成CO2和水蒸气外,试管中还有一些黑色粉末状固体。他们通过实验探究,分析黑色固体的组成,并验证产生的气体。请填空:
(1)提出问题:黑色固体是什么?
(2)猜想与假设:黑色团体可能是:a、炭粉 b、氧化铜 c、_____ 。
(3)查阅资料:炭粉和氧化铜均为黑色固体,其中炭粉不与稀酸反应,也不溶于稀酸,而氧化铜可与稀酸反应而溶解。
(4)设计实验方案:向试管中的黑色团体滴加足量的_____(填化学式)溶液,充分反应后,观察固体的溶解情况和所得溶液的颜色。
(5)现象与结论:如果猜想 a 正确,则现象为____; 若现象是_____,则猜想 b正确;反应的化学方程式:_________。假如现象为_______,则猜想 c 成立。
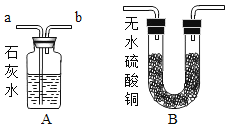
(6)若用如图装置验证两种气体生成物,应将生成的混合气体先通过____装置。当将气体通入装置A 进行验证时,化学方程式为_____。
【答案】炭粉和氧化铜 H2SO4或HCl 固体不溶解,溶液没有明显变化 固体全部溶解,溶液由无色变成蓝色 ![]() 或
或![]() 固体部分溶解,溶液由无色变成蓝色 B
固体部分溶解,溶液由无色变成蓝色 B ![]()
【解析】
由题意探究铜绿[![]() ]受热分解后黑色固体的组成,并验证产生的气体。
]受热分解后黑色固体的组成,并验证产生的气体。
(2)猜想与假设:根据质量守恒定律,化学反应前后,元素的种类不变,![]() 中含铜、氢、氧、碳元素,炭粉和氧化铜均为黑色固体,故黑色固体可能是炭粉,氧化铜,或炭粉与氧化铜的混合物,故猜想c为炭粉和氧化铜;
中含铜、氢、氧、碳元素,炭粉和氧化铜均为黑色固体,故黑色固体可能是炭粉,氧化铜,或炭粉与氧化铜的混合物,故猜想c为炭粉和氧化铜;
(4)根据资料信息,由于炭粉不与稀酸反应,也不溶于稀酸,而氧化铜可与稀酸反应而溶解,设计实验方案:向试管中的黑色固体滴加足量的H2SO4(或HCl)溶液,根据反应现象,可以推断固体的组成,充分反应后,观察到部分固体的溶解溶液变为蓝色说明既有炭粉又有氧化铜,固体不溶解说明只有炭粉,固体全部溶解溶液变为蓝色说明只有氧化铜,根据固体溶解情况和所得溶液的颜色,可判定黑色固体成分;
(5)现象与结论:若猜想a正确,则固体为炭粉,加酸不溶解溶液仍为无色;若猜想 b正确,则固体为氧化铜,加酸固体全部溶解,溶液由无色变为蓝色,氧化铜与稀硫酸反应生成硫酸铜和水,反应的化学方程式为![]() ,氧化铜与稀盐酸反应生成氯化铜和水,反应的化学方程式为
,氧化铜与稀盐酸反应生成氯化铜和水,反应的化学方程式为![]() ;猜想c成立,黑色固体为炭粉和氧化铜的混合物,炭粉不与稀酸反应,也不溶于稀酸,氧化铜能与稀酸反应成硫酸铜或氯化铜,硫酸铜溶液或氯化铜溶液为蓝色,故实验现象为固体部分消失,溶液由无色变为蓝色;
;猜想c成立,黑色固体为炭粉和氧化铜的混合物,炭粉不与稀酸反应,也不溶于稀酸,氧化铜能与稀酸反应成硫酸铜或氯化铜,硫酸铜溶液或氯化铜溶液为蓝色,故实验现象为固体部分消失,溶液由无色变为蓝色;
(6)若用如图装置验证两种气体生成物CO2和水蒸气,若先验证二氧化碳,气体会从澄清石灰水中带出水蒸气,从而使无水硫酸铜变蓝,无法验证混合气体中是否含有水;应先将生成的混合气体先通过B装置,无水硫酸铜遇水变蓝,可以验证混合气体中的水蒸气;再通过A装置验证二氧化碳,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,使澄清石灰水变浑浊,反应的化学方程式为![]() 。
。

【题目】甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如下表所示:
物质 | 甲烷 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 3.2 | 11.2 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
下列判断正确的是
A.表中a的值为2.6 B.X一定是该反应的催化剂
C.X可能含有氢元素 D.X一定含有氧元素
【题目】取四份等质量的KClO3,向其中三份中分别加入少量等质量的KMnO4、MnO2和Mn,分别在某温度下加热至质量不再改变,测定产生氧气的质量。然后将剩余固体溶于足量水中,添加过少量物质的组别中均有相同组成的不溶物。测定结果如下:
组别 | ① | ② | ③ | ④ |
加入的物质 | 无 | KMnO4 | MnO2 | Mn |
产生氧气的质量 | m | m1 | m2 | m3 |
不溶物的质量 | 0 | w1 | w2 | w3 |
已知:含钾的化合物均溶于水;![]() ,下列关于此实验的说法一定正确的是( )
,下列关于此实验的说法一定正确的是( )
A.KMnO4是KClO3分解制氧气的最佳催化剂
B.残留不溶性物质的质量关系为w1<w2<w3
C.不加入其他物质时,KClO3不会发生分解反应
D.产生氧气的质量关系为m1<m2<m3
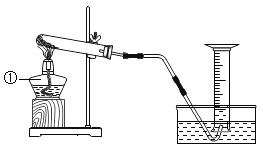
【题目】某兴趣小组对KClO3分解反应的催化剂进行研究,在相同的加热条件下,用下图装置完成表中实验。
编号 | KClO3质量/g | 催化剂 | 催化剂质量/g | 收集50mLO2所需时间/s |
实验1 | 5 | - | - | 171 |
实验2 | 5 | MnO2 | 0.5 | 49 |
实验3 | 5 | Fe2O3 | 0.5 | 58 |
实验4 | 5 | KCl | 0.5 | 154 |
(1)仪器①的名称为____________。
(2)实验室用KClO3制取氧气的化学方程式为_______________________________。
(3)表中所列3种催化剂的催化效果最佳的是____________。
(4)由实验1和实验4可知,KCl对KClO3分解______(填“有”或“无”)催化作用。
(5)要比较KClO3分解反应中不同催化剂的催化效果,除了测量收集50mLO2所需时间外,还可以测量相同时间内____________。
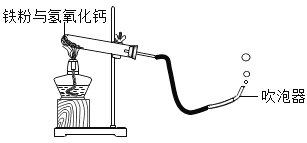
【题目】用如图装置进行铁与水蒸气在较高温度下反应的实验。取适量的铁粉与氢氧化钙平铺在试管底部,点燃酒精灯,待有较大气泡产生时,用燃着的木条靠近气泡直至有爆鸣声。
(提出问题)改变铁粉和氢氧化钙的质量及两者放置的方式是否会影响实验效果呢?
(查阅资料)①Ca(OH)2![]() CaO+H2O↑
CaO+H2O↑
②“气泡爆鸣时间”指从开始加热到第一个气泡爆鸣所用的时间
③“气泡爆鸣时间”越短,实验效果越好
(进行实验)按下表进行实验,记录“气泡爆鸣时间”。
表1
实验 | 铁粉与氢氧化钙的放置方式 | 铁粉的质量/g | 氢氧化钙的质量/g | 气泡爆鸣时间/s |
1 | 铁粉在上层 | 0.5 | 1.5 | 151 |
2 | 1.0 | 1.0 | 119 | |
3 | 1.5 | 0.5 | 66 | |
4 | 铁粉在下层 | 0.5 | 0.5 | 88 |
5 | 1.0 | a | 44 | |
6 | 1.5 | 1.0 | 54 | |
7 | 二者均匀混合 | 0.5 | 1.0 | 77 |
8 | 1.0 | 0.5 | 58 | |
9 | 1.5 | 1.5 | 60 |
(处理数据)根据表1,计算“气泡爆鸣时间”均值,结果如下:
表2
因素 | 放置方式 | 铁粉的质量/g | 氢氧化钙的质量/g | ||||||
铁粉 在上层 | 铁粉 在下层 | 均匀混合 | 0.5 | 1.0 | 1.5 | 0.5 | 1.0 | 1.5 | |
气泡爆鸣时间均值/s | 112 | 62 | 65 | 105 | 74 | 60 | 70 | 83 | 85 |
(解释与结论)
(1)实验中,使用氢氧化钙的目的是____。
(2)实验中,生成的气体为氢气,其理由是____。
(3)表1中,a为____g。
(4)根据表2推断,最佳的实验条件为___。
(反思与评价
(5)表2中,1.5 g铁粉对应的均值为60。计算该值依据的3个数据分别是______。
(6)实验中,铁粉在下层比上层的实验效果好。从金属性质的角度解释原因:______。