题目内容
【题目】下列四个图象分别对应四种操作过程,其中正确的是( )
A.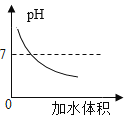 用水稀释KOH溶液
用水稀释KOH溶液
B.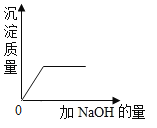 向盐酸和氯化铜混合液中加入NaOH溶液,直到过量
向盐酸和氯化铜混合液中加入NaOH溶液,直到过量
C.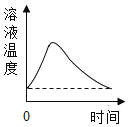 室温时,向一定量的水中加入少量CaO
室温时,向一定量的水中加入少量CaO
D.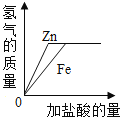 常温下,把等质量的锌和铁分别与等质量分数的足量稀盐酸反应
常温下,把等质量的锌和铁分别与等质量分数的足量稀盐酸反应
【答案】C
【解析】
A、用水稀释KOH溶液时,pH减小至无限接近于7,但是不能减小到7,更不能小于7,该选项对应关系不正确,不符合题意;
B、向盐酸和氯化铜混合液中加入NaOH溶液时,氢氧化钠先和盐酸反应生成氯化钠和水,待盐酸完全反应后,氢氧化钠再和氯化铜反应生成氢氧化铜沉淀和氯化钠,故一开始无沉淀产生,之后,沉淀的质量逐渐增加,待氯化铜完全反应后,不再变化,该选项对应关系不正确,不符合题意;
C、室温时,向一定量的水中加入少量CaO,氧化钙和水反应生成氢氧化钙,放热,温度升高,完全反应后温度降低,直至降低至原温度,符合题意;
D、常温下,把等质量的锌和铁分别与等质量分数的足量稀盐酸反应时,根据化学方程式![]() ,
, ![]() 可知,每65份质量的锌生成2份质量的氢气,每56份的铁生成2份质量的氢气,故最终铁和稀盐酸反应生成的氢气多,该选项对应关系不正确,不符合题意。
可知,每65份质量的锌生成2份质量的氢气,每56份的铁生成2份质量的氢气,故最终铁和稀盐酸反应生成的氢气多,该选项对应关系不正确,不符合题意。
故选C。

 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案【题目】一瓶敞口放置的NaOH,设计实验证明它是部分变质的___,并写出实验过程中发生反应的化学方程式____,若要把变质后的杂质除去得到较纯净的NaOH溶液,写出除杂发生反应的化学方程式_____。
【题目】某食用碱的主要成分是 ![]() ,其中含有少量的 NaCl,小明同学为测定该食用碱中
,其中含有少量的 NaCl,小明同学为测定该食用碱中 ![]() 的质量分数,他进行了以下实验,取60g食用碱,加水配成400g的溶液,把溶液平均分为四份,然后分别加入一定质量分数的
的质量分数,他进行了以下实验,取60g食用碱,加水配成400g的溶液,把溶液平均分为四份,然后分别加入一定质量分数的![]() 溶液,实验数据见表:
溶液,实验数据见表:
实验一 | 实验二 | 实验三 | 实验四 | |
食用碱溶液的质量 | 100g | 100g | 100g | 100g |
加入 | 20g | 40g | 60g | 80g |
生成沉淀的质量 | 3g | 6g | m | 10g |
请分析表中数据并计算回答。
(1)m=______;
(2)该60g食用碱配成的溶液与足量![]() 溶液反应,最多生成沉淀质量为_______g;
溶液反应,最多生成沉淀质量为_______g;
(3)该食用碱中 ![]() 的质量分数是多少_______?(写出计算过程,答案精确到
的质量分数是多少_______?(写出计算过程,答案精确到 ![]() )
)