题目内容
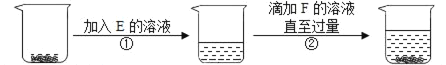
【题目】某金属冶炼厂的管道烟泥中含有少量铜、锌、硫等单质。现欲回收铜和锌,并对硫进行环保处理,主要步骤如下图所示:
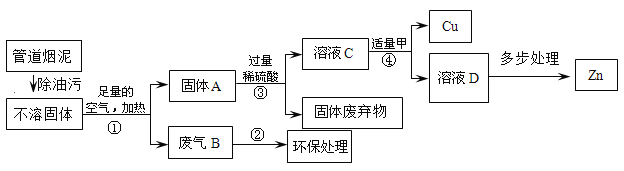
已知:加热的条件下,Zn、Cu都可以与氧气反应生成相应的金属氧化物。
(1)烟泥最初处理需要除油污,用洗涤剂除油污的过程中发生了__________现象。步骤①产生的废气B中,一定含有的有害气体是______(填化学式)。环保处理最好釆用的试剂是__________(填字母序号)。
A浓硫酸 B食盐水 C石灰乳
(2)写出步骤④中得到铜的化学方程式______,它属于基本反应类型中的_____反应。
(3)步骤③和④中主要操作的名称是__________。
(4)我国古代就制得了一种外观似金子的锌和铜的合金,也就是黄铜,它的硬度比纯铜__________(填“高”或者“低”)。
(5)取少量的溶液C,往其中加入一定质量的镁粉,充分反应后过滤,得到滤渣和滤液。往滤渣中加入稀盐酸有气泡产生,则滤液中一定没有__________(填字母序号)。
A硫酸镁 B硫酸锌 C硫酸铜 D硫酸铜和硫酸锌
【答案】乳化 SO2 C Zn+CuSO4=Cu+ZnSO4 置换 过滤 高 C
【解析】
(1)烟泥最初处理需要除油污,用洗涤剂除油污的过程中发生了乳化现象。烟泥中存在单质硫,在空气中加热时会产生二氧化硫,二氧化硫是常见的空气污染物,化学式为SO2。二氧化硫和浓硫酸、食盐水不发生反应,与石灰乳(化学式为Ca(OH)2)反应生成亚硫酸钙沉淀和水。故选C。
(2)写出步骤④中得到铜的化学方程式Zn+CuSO4=Cu+ZnSO4,它属于基本反应类型中的置换反应。
(3)步骤③和④中主要操作的名称是过滤。
(4)合金的硬度比组成其组分的纯金属的硬度大,故锌和铜的合金,也就是黄铜,它的硬度比纯铜高。
(5)溶液C中含有硫酸锌和硫酸铜,往其中加入一定质量的镁粉,镁先和硫酸铜反应生成硫酸镁和铜,若镁过量,再和硫酸锌反应生成硫酸镁和锌,充分反应后过滤,得到滤渣和滤液。往滤渣中加入稀盐酸有气泡产生,说明滤渣中一定有铜、锌,可能有镁,则滤液中一定没有硫酸铜,故选C。

 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案【题目】某化学兴趣小组的同学对一批铁样品(含有杂质,杂质不溶于水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中只有一位同学所用的稀硫酸与铁样品恰好完全反应。实验数据如下表:
甲 | 乙 | 丙 | |
稀硫酸 | 150 | 120 | 120 |
铁样品 | 12 | 12 | 15 |
反应后的剩余物 | 161.6 | 131.6 | 134.6 |
(1)____同学所用的稀硫酸与铁样品恰好完全反应;共产生___ g气体。
(2)计算样品中的铁的质量分数是_____?(最后结果精确到0.1%,下同)
(3)计算恰好完全反应后所得溶液中溶质的质量分数____?