题目内容
【题目】(6分)为了维护南海权益,我国去年宣布成立了三沙市。这是维护国家主权的象征,同时也是因为海洋资源十分丰富,有广泛的利用价值。其中通过海水晾晒即可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
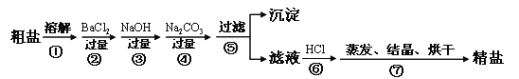
(1)根据以上信息,请写出海水中所含的主要阴离子的符号 。
(2)在上述流程中第③步加过量NaOH的目的是除去海水中的 (填离子符号,下同),第④步加过量Na2CO3的目的是除去海水中的 。第⑥步其实显示的是加适量盐酸,其目的是除去多余的 。
(3)请写出第②步所发生反应的化学方程式 。
(4)在第③步操作中,选择的除杂试剂不能用KOH代替NaOH,理由是 。
【答案】(1)Cl- 、SO42-
(2)Mg2+ 、Ca2+ ; CO32- 、OH-
(3)BaCl2 + Na2SO4 = BaSO4↓+ 2NaCl
(4)用KOH会引入新杂质。
【解析】
试题分析:(1)由题意可知,海水中所含的主要阴离子是Cl-、SO42-;
(2)由于氯化镁与氢氧化钠的反应生成了氢氧化镁沉淀.所以,第③步加过量NaOH的目的是除去海水中的Mg2+;由于氯化钙与碳酸钠的反应生成了碳酸钙沉淀,所以,第④步加过量Na2CO3的目的是除去海水中的 Ca2+;由于盐酸与碱、碳酸盐的反应,所以,第⑥步其实显示的是加适量盐酸,其目的是除去多余的OH-、CO32-;
(3)在第②步中硫酸钠与氯化钡反应生成了硫酸钡沉淀和氯化钠,反应的方程式是:Na2SO4+BaCl2=BaSO4↓+2NaCl;
(4)在第③步操作中,选择的除杂试剂不能用KOH代替NaOH,理由是:如果用KOH代替NaOH,最得到的精盐中含有氯化钾.

【题目】(15分)某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
【查阅资料】
①生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质(不与酸反应).
②生产原理反应:NaCl+ NH3 + CO2 + H2O= NaHCO3↓+ NH4Cl,分离得晶体B,并使其充分受热,可分解制得纯碱,同时得到二氧化碳和水.
③氯化铵分解的化学方程式是NH4Cl △ NH3↑+HCl↑.
④部分生产流程如下图所示:
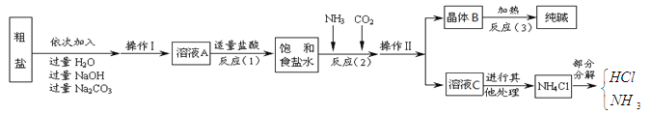
【问题讨论】
(1)①溶液A中的溶质有NaCl和 、 ,
②操作Ⅱ的名称为 .
③流程中Na2CO3溶液的作用是除去粗盐中的 .
④写出加入NaOH溶液与MgCl2反应的化学方程式 .
⑤晶体B受热分解的化学方程式为 .
(2)上述生产流程中可循环使用的是 (填序号).
A.NaOH B.NH3 C.HCl D.CO2
【组成探究一】
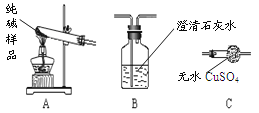
(3)设计实验检验纯碱样品中是否混有晶体B,请完成下表
选择的装置 | 实验现象 | 实验结论 |
选择的装置(填序号) | 实验现象 | 实验结论 |
样品不含晶体B |
【组成探究二】
(4)取纯碱样品加水溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.产生沉淀的方程式为 ,由此确定纯碱样品含有杂质NaCl.
【组成探究三】
(5)同学们为了测定该纯碱样品的纯度,设计了如下实验:
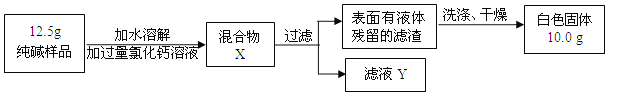
①判断加入氯化钙溶液是否过量的方法是 ,然后观察现象判断.
②判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加 ,然后观察现象判断.
A.氯化钡溶液 B.硝酸银溶液 C.碳酸钠溶液 D.稀盐酸
③根据实验数据,计算样品中碳酸钠的质量分数是多少?(写出计算过程.3分)