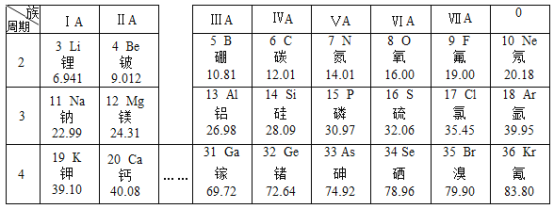
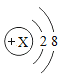题目内容
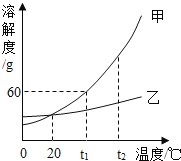
【题目】在氢氧化钠溶液中逐滴滴加稀盐酸。实验过程中溶液温度的变化及实验操作如图一、图二所示:

(1)在氢氧化钠溶液中滴加无色酚酞的作用是_____。
(2)根据图二所示:AB段曲线上升的原因是_____;C点时溶液中所含的阳离子有__。
(3)已知氢氧化钠稀溶液的浓度和相应的pH值如下表所示:
①根据下表推断,当溶液的pH值近似为12时,氢氧化钠溶液的溶质质量分数为___。
溶液中氢氧化钠的质量分数 | 近似pH值 |
4% | 14 |
0.4% | 13 |
12 | |
0.004% | 11 |
0.0004% | 10 |
②计算在50g溶质质量分数为4%的氢氧化钠溶液中,加入30g浓度为3.65%的稀盐酸,充分反应后所得溶液中氢氧化钠的质量分数为________,所得溶液的pH范围是_____ (填字母)。
A 10~11 B 11~12 C 12~13 D 13~14
(4)某造纸厂有10 t含NaOH的质量分数为3.2%的废水,现要用溶质质量分数为3.65%盐酸进行处理至中性后排放,需要这种盐酸的多少吨____?(废水中其他物质不与盐酸反应,写出计算过程)
【答案】通过其颜色变化,帮助判断反应发生 中和反应放出热量 Na+、H+ 0.04% 1% D 8t
【解析】
(1)无色酚酞的作用是通过其颜色变化,帮助判断反应发生;
(2)氢氧化钠和盐酸反应生成氯化钠和水,属于中和反应,此反应过程中放出热量;C点是盐酸过量,溶液中溶质是氯化钠、氯化氢,阳离子是Na+、H+;
(3)①分析表中数据可知,当溶液的pH值近似为12时,氢氧化钠溶液的溶质质量分数为0.04%;
②设参加反应的氢氧化钠的质量为x,

![]()
x=1.2g,
充分反应后所得溶液中氢氧化钠的质量分数为![]() ,所以溶液的pH范围是 13~14;
,所以溶液的pH范围是 13~14;
(4)设需要这种盐酸的质量为y,

![]()
y=8t。

练习册系列答案
相关题目