题目内容
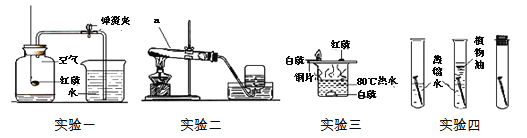
【题目】(6分)观察下图并回答问题:

由上图可知,HCl与NaOH的反应实质是H+ 和OH- 之间的反应,此反应可表示为:H++0H-=H2O。像这种用实际参与反应的离子来表示反应的式子称为离子方程式。任何复分解反应都可用离子方程式来表示。
[练习] 按照书写化学方程式的要求写出下列反应的离子方程式
HCl溶液与AgNO3 溶液反应: 。
HNO3溶液与Na2CO3溶液反应: 。
[归纳] 复分解反应的实质是:阴阳离子结合生成 的反应。
[应用] 判断在水溶液中一定能大量共存的离子组是 。
a、Na+、H+、Cl-、CO32- b、H+、Ba2+、Cl-、SO42-
c、Cu2+、Na+、NO3-、OH- d、H+、K+、Cl-、SO42-
【答案】[练习] Ag+ + Cl- = AgCl↓ 2H+ + CO32- = CO2↑+ H2O
[归纳] 沉淀、气体和水 [应用] d
【解析】
试题分析:[练习] HCl溶液与AgNO 溶液反应的离子方程式:Ag+ + Cl- = AgCl↓;
HNO3溶液与Na2CO3溶液反应的离子方程式:2H+ + CO32- = CO2↑+ H2O
[归纳] 复分解反应的实质是:阴阳离子结合生成沉淀、气体和水的反应
[应用] a、H+和CO32-相互结合形成H2CO3,不稳定会分解成二氧化碳和水,b、Ba2+和SO42-相互结合形成白色沉淀BaSO4,c、Cu2+和OH-相互结合形成蓝色沉淀Cu (OH)2,d可以大量共存,故选d

 名校课堂系列答案
名校课堂系列答案【题目】如表是硝酸钾、氯化钠在不同温度下的溶解度.
温度/℃ | 10 | 20 | 30 | 40 | 50 |
硝酸钾的溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 |
氯化钠的溶解度/g | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(1)从表中数据分析,溶解度受温度影响较大的物质是__________,硝酸钾和氯化钠溶解度曲线的交点在 __________(填字母序号)之间.
A.20℃~30℃ B.30℃~40℃ C.40℃~50℃
(2)20℃,将50g硝酸钾与100g水混合,充分搅拌后静置,得到的溶液是硝酸钾的__________(“饱和”或“不饱和”)溶液,若将温度升高到40℃,该溶解溶质的质量分数为__________(精确到0.1%).
(3)保持温度为20℃,将氯化钠的不饱和溶液变成饱和溶液,写出一种可行的方法__________。