题目内容
【题目】请根据如图A、B、C三种物质的溶解度曲线,回答下列问题:
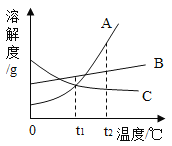
(1)温度越高,溶解度越小的物质是___________________;
(2)t1℃时,物质A和C的溶解度均为25g,其饱和溶液中溶质的质量分数为____________.
(3)t℃时,把等质量的A和C配成饱和溶液,A的饱和溶液质量大于C,温度t的范围是_____________.
(4)下列说法正确的是___________(填序号).
①将t1℃的A、B、C三种溶液分别升温,其浓度都不可能发生变化
②将t1℃的A、B、C三种溶液分别降温,其浓度都可能发生变化
③将t2℃的A、B、C三种饱和溶液的温度分别降至t1℃时,A溶液中析出的晶体最多
④在温度为t2℃时,A、B、C三种溶液的溶质质量分数可能相等
【答案】C 20% 小于t1℃ ④
【解析】
(1)通过分析溶解度曲线可知,温度越高,溶解度越小的物质是:C;
(2)t1℃时,物质A和C的溶解度均为25g,其饱和溶液中溶质的质量分数为:![]() ×100%=20%;
×100%=20%;
(3)t℃时,把等质量的A和C配成饱和溶液,A的饱和溶液质量大于C,说明A物质的溶解度小于C物质的溶解度,所以温度t的范围是小于t1℃;
(4)①将t1℃的A、B、C三种溶液分别升温,C物质的溶解度随温度的升高而减小,C物质可能析出晶体,溶质质量分数可能减小,故错误;
②将t1℃的A、B、C三种溶液分别降温,A、B物质的溶解度随温度的降低而减小,降低温度,达到饱和状态后,可能会析出晶体,所以浓度可能发生变化,C物质的浓度不会变化,故错误;
③将t2℃的A、B、C三种饱和溶液的温度分别降至t1℃时,A物质的溶解度变化最大,没说溶液质量相等,所以A溶液中析出的晶体不能确定,故错误;
④在温度为t2℃时,A、B、C三种溶液的溶质质量分数可能相等, C饱和,A、B不饱和时,溶质质量分数可能相等,故正确。

【题目】某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动。
(提出问题)这种淡黄色粉末是什么?有什么性质和用途?
(查阅资料)①硫是淡黄色粉末,不溶于水;②过氧化钠(Na2O2)是淡黄色粉末,在常温下能与水反应生成碱和一种气体;在呼吸面具中和潜水艇里常用作供氧剂。
(猜想与探究)猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物。
探究:过氧化钠与水反应的生成物的成分。
(实验与结论)
实验操作 | 实验现象 | 实验结论 | |
猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水 |
| 猜想a、c不成立,猜想b成立。 |
探究 | ①用带火星的木条伸入过氧化钠与水反应的试管中 | 木条复燃 | 生成物有___________ |
②往①试管内的溶液中滴加___________ |
| 生成物有氢氧化钠 |
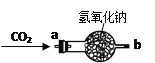
(继续探究)小组的同学对过氧化钠能作为供氧剂也很感兴趣,大家讨论认为可能是CO2在常温下能与过氧化钠反应有关,于是设计右图所示的装置继续实验探究。
实验操作 | 实验现象 | 实验结论 |
①将CO2从a口处通入装置内,再把带火星的木条放在装置b口处 | 木条复燃 | CO2在常温下能与过氧化钠反应,该反应的化学方程式为: |
②取出充分反应后的固体生成物于试管中,往试管内滴加稀盐酸,将生成的氢气通入澄清石灰水中 | 有气泡产生 |
(交流与比较)与我们学过的制氧气方法相比,常选用过氧化钠作为呼吸面具和潜水艇的供氧剂的主要理由是(从两个不同角度回答):________________________________、________________________________。