题目内容
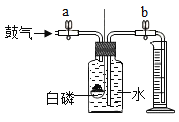
【题目】某研究性学习小组在验证"铝丝与硫酸铜溶液反应"的实验时,发现很长一段时间铝丝表面都没有明显的现象。
[ 提出问题 ] 是什么原因导致反应现象不明显呢?
[ 查阅资料 ] 氯离子穿透铝表面致密氧化膜的能力强于硫酸根离子。
[ 猜想与假设 ]
甲:可能与反应物间的接触面积有关;
乙:可能与硫酸根离子穿透氧化膜的能力有关;你认为还可能与_________有关( 写出一条即可 )。
[设计实验 ]
(1)将打磨后的等质量的铝片和铝丝分别放入等体积、浓度的硫酸铜溶液中,发现前者反应的速率明显比后者快,观察到的现象是__________。甲认为自己的猜想正确。
(2) 你认为该实验设计是_________(填“严谨" 或“不严谨”)的,理由是________。请写出铝与硫酸铜溶液反应的化学方程式___________。
(3)设计实验验证乙的猜想:
实验操作 | 实验现象 | 实验结论 |
室温下,将两根相同的铝丝分别放入等体积、浓度的硫酸铜溶液和______________溶液中 | 后者铝丝表面变红明显比前者快 | 乙同学猜想正确 |
(4)若要进一步验证乙的猜想,请完成下列实验方案;
实验操作 | 实验现象 | 实验结论 |
_________ | _________ | 乙同学猜想正确 |
【答案】硫酸铜溶液的浓度或温度 溶液变浅,最后变为无色,铝的表面有红色物质析出 ( 答案合理即可 ) 不严谨 没有控制温度相同 ( 答案合理即可 ) ![]() 氯化铝 取与上述实验等体积,等浓度的硫酸铜溶液置于试管中,再加入少量氯化铝完全溶解,取与上述实验打磨程度相同的铝丝插入试管中,观察现象 立即有红色固体析出,溶液由蓝色逐渐变为无色
氯化铝 取与上述实验等体积,等浓度的硫酸铜溶液置于试管中,再加入少量氯化铝完全溶解,取与上述实验打磨程度相同的铝丝插入试管中,观察现象 立即有红色固体析出,溶液由蓝色逐渐变为无色
【解析】
{猜想与假设}化学反应受多种因素的影响,铝丝与硫酸铜溶液反应的速率不仅与铝的形状有关,还受硫酸铜溶液的浓度或温度影响,故填硫酸铜溶液的浓度或温度。
{设计实验}(1)铝与硫酸铜反应生成硫酸铝和铜,实验中观察到的现象是溶液由蓝色逐渐变成无色,同时铝的表面有红色物质析出,故填溶液变浅,最后变为无色,铝的表面有红色物质析出。
(2)该实验的设计是不严谨的,故填不严谨;
实验中只控制了硫酸铜溶液的体积与浓度,没有控制硫酸铜溶液的温度,所以实验设计不严谨,故填没有控制温度相同;
铝与硫酸铜反应生成硫酸铝和铜,故反应的化学方程式写为:2Al+3CuSO4=Al2(SO4)3+3Cu。(3)乙同学的猜想正确,则实验中的药品中应该含有氯离子,所以需要的药品是氯化铝溶液,故填氯化铝。
(4)要进一步验证乙的猜想,还可以采用以下实验方案:取与上述实验等体积,等浓度的硫酸铜溶液置于试管中,再加入少量氯化铝完全溶解,取与上述实验打磨程度相同的铝丝插入试管中,观察现象,故填取与上述实验等体积,等浓度的硫酸铜溶液置于试管中,再加入少量氯化铝完全溶解,取与上述实验打磨程度相同的铝丝插入试管中,观察现象;
该实验中观察到的现象是立即有红色固体析出,溶液由蓝色逐渐变为无色,说明乙同学的猜想正确,故填立即有红色固体析出,溶液由蓝色逐渐变为无色。

【题目】兴趣小组的利用提供的试剂:稀硫酸、澄清石灰水、氯化钠溶液、硫酸铜溶液和紫色石蕊溶液。探究酸碱盐的性质。小清同学将氯化钠溶液加入到稀硫酸中没有观察到明显现象,而将混合溶液加热一段时间后,意外地闻到刺激性气味。
[提出问题]刺激性气味的气体是什么?
[猜想与假设]猜想1.可能是二氧化硫 猜想2.可能是氯化氢
猜想3.可能是氨气
大家讨论后认为猜想3不合理,依据是_____________________。
[查阅资料] SO2和CO2的化学性质相似,都能使澄清灰水变浑浊。写出二氧化硫和氢氧化钙的反应的化学方程式:____________________________。
[实验探究]如图所示,小诚将产生的气体通入紫色石蕊溶液中,观察到_________,于是他认为猜想2正确。
[评价与改进]小煜认为小诚的结论不科学,于是他利用提供的试剂通过实验确认了猜想2正确。
实验操作 | 实验现象 |
如图所示,将产生的气体________________ | _____________________ |
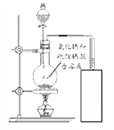
[结论]加热氯化钠与硫酸的混合溶液得到的气体是氯化氢
[拓展应用]实验室可用氯化钠和硫酸反应制取氯化氢气体,已知氯化氢气体极易溶于水。请推测实验室制取氯化氢气体最适宜的方法为________________(填序号)。
A.加热氯化钠溶液和稀硫酸的混合物 B.加热氯化钠固体和稀硫酸的混合物
C.加热氯化钠固体和浓硫酸的混合物