题目内容
【题目】A~K是初中化学常见的物质,相互转化关系如图所示,已知A是气体,B是红褐色的固体,K是常用的补钙剂的主要成份。H常用于工业生产玻璃。
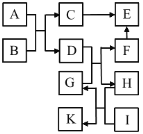
(1)F的化学式是______________。
(2)I的一种用途是______________。
(3)由H+I→G+K的化学方程式为:______________。
(4)以上反应中一定不包括的反应类型是______________。
【答案】H2O 建筑材料(中和酸性土壤;处理酸性污水等合理即可) Na2CO3+Ca(OH)2=CaCO3↓+2NaOH 化合反应
【解析】
A是气体,B是红褐色的固体,A与B能够反应生成C和D,则A是一氧化碳,B是氧化铁,C与D分别是铁和二氧化碳中的一种;K是常用的补钙剂的主要成份,则K是碳酸钙;H常用于工业生产玻璃,且能与I反应生成K(碳酸钙),则H是碳酸钠,I是氢氧化钙,G为氢氧化钠;G与D反应生成H(碳酸钠)和F,所以D为二氧化碳,C为铁,F为水;F(水)和C(铁)都能发生化学反应生成E,则E为氢气。
(1)由分析可知,F为水,其化学式为H2O,故填H2O。
(2)由分析可知,I为是氢氧化钙,氢氧化钙可做建筑材料,还能用于改良酸性土壤、处理酸性污水等,故填建筑材料或中和酸性土壤或处理酸性污水等。
(3)由分析可知,H是碳酸钠,I是氢氧化钙,G是氢氧化钠,K是碳酸钙,即H+I→G+K的反应是碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,故反应的化学方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH。
(4)由分析可知,A与B反应是氧化铁与一氧化碳反应生成铁和二氧化碳,不属于任何反应类型,D和G的反应是氢氧化钠与二氧化碳反应生成碳酸钠和水,不属于任何反应类型,H和I的反应是碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,属于复分解反应,F生成E的反应是水在通电的条件下反应生成氢气和氧气,属于分解反应,C生成E的反应是铁与酸反应生成亚铁盐和氢气,属于置换反应,所以图中的反应中一定不包括的反应类型是化合反应,故填化合反应。

【题目】某研究性学习小组在验证"铝丝与硫酸铜溶液反应"的实验时,发现很长一段时间铝丝表面都没有明显的现象。
[ 提出问题 ] 是什么原因导致反应现象不明显呢?
[ 查阅资料 ] 氯离子穿透铝表面致密氧化膜的能力强于硫酸根离子。
[ 猜想与假设 ]
甲:可能与反应物间的接触面积有关;
乙:可能与硫酸根离子穿透氧化膜的能力有关;你认为还可能与_________有关( 写出一条即可 )。
[设计实验 ]
(1)将打磨后的等质量的铝片和铝丝分别放入等体积、浓度的硫酸铜溶液中,发现前者反应的速率明显比后者快,观察到的现象是__________。甲认为自己的猜想正确。
(2) 你认为该实验设计是_________(填“严谨" 或“不严谨”)的,理由是________。请写出铝与硫酸铜溶液反应的化学方程式___________。
(3)设计实验验证乙的猜想:
实验操作 | 实验现象 | 实验结论 |
室温下,将两根相同的铝丝分别放入等体积、浓度的硫酸铜溶液和______________溶液中 | 后者铝丝表面变红明显比前者快 | 乙同学猜想正确 |
(4)若要进一步验证乙的猜想,请完成下列实验方案;
实验操作 | 实验现象 | 实验结论 |
_________ | _________ | 乙同学猜想正确 |
【题目】某实验小组在做“用澄清石灰水检验二氧化碳”的实验时,发现一个有趣的实验现象:
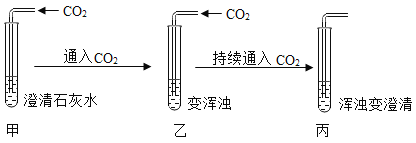
[提出问题]澄清石灰水通入二氧化碳会变浑浊,持续通入二氧化碳,浑浊变澄清,丙试管中溶液的溶质成分是什么?
[查阅资料]
①碳酸钙不溶于水,碳酸钙能与二氧化碳、水反应生成碳酸氢钙[ Ca(HCO3)2]。
②碳酸氢钙易溶于水,受热易分解,生成碳酸钙、二氧化碳、水。
③碳酸氢钙能与氢氧化钠溶液反应生成碳酸钙,能与盐酸反应生成二氧化碳。
[假设与猜想]
猜想1:碳酸钙;
猜想2 :碳酸氢钙和氢氧化钙;
猜想3:只有__________。
[思考与讨论]
同学们认为猜想①一定不正确,理由是____________;小王同学认为猜想2也不正确,理由是___________。
[实验探究]
实验 | 实验步骤 | 实验现象 | 结论 |
一 | 取丙中少量液体于试管中,滴加__ | 有气泡生成 | 猜想3成立 |
二 | 取丙中少量液体于试管中,滴加氢氧化钠溶液 | 有___生成 | |
三 | 取丙中少量液体于试管中,加热 | _________ |
[反思交流]
①由实验可知,反应中产生的现象与______有关;
②试管丙中浑浊变澄清的反应方程式为_____________。