题目内容
【题目】利用图1装置进行I、II两组实验,将滴管a中的液体滴入b中,待充分作用后,打开止水夹d。a、b、c中所加试剂如下表所示。
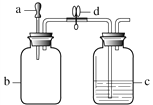
图1
实验 | a中试剂 | b中试剂 | c中试剂 |
I | 5%H2O2溶液 | MnO2 | 80 ℃热水 |
II | 石蕊溶液 | HCl气体 | NaOH溶液 |
已知:HCl气体极易溶解于水。白磷的着火点为40 ℃。
(1)实验I中,若在c中长导管口处放置一块白磷,当打开止水夹后,可观察到白磷燃烧,通过此实验能证明燃烧的条件是________。 若要证明燃烧的另一条件,在对比实验中,需将c中盛放的试剂改为________。
(2)实验II能证明NaOH与HCl发生了反应。实验过程中,打开止水夹d后,可观察到的现象为________。
(3)若按图2所示连接装置,进行实验II,则会观察到c中长导管口有气泡产生,原因是________。

图2
【答案】 与氧气接触 冷水 c中的水到吸入b中,b中红色溶液变成蓝色(或紫色) b中HCl气体溶于水,导致瓶内压强低于大气压,使瓶外空气进入c中
【解析】(1)根据燃烧的条件(可燃物、氧气、温度达到可燃物着火点)分析解答;
(2)根据HCl气体极易溶解于水,压强降低及酸碱中和分析解答;
(3)根据HCl气体极易溶解于水,压强降低分析解答。
解:(1)a中的5%H2O2溶液加入到装有MnO2的b中,生成氧气。当打开止水夹后,氧气经c排出。而c中液体温度为80 ℃热水,故排出的氧气温度超过白磷的着火点为40 ℃。若在c中长导管口处放置一块白磷,可观察到白磷燃烧,通过此实验能证明燃烧的条件是:与氧气接触;若要证明燃烧的另一条件,在对比实验中,需将c中盛放的试剂改为冷水;
(2)a中的石蕊溶液加入到装有HCl气体的b中,b中溶液变红。由于HCl气体极易溶解于水,导致b中压强降低,从而使c中氢氧化钠溶液倒吸入b中,与HCl
反应,溶液酸性降低。b中红色溶液变成蓝色(或紫色)。故可观察到的现象为c中的氢氧化钠溶液倒吸入b中,b中红色溶液变成蓝色(或紫色);
(3)由于HCl气体极易溶解于水,压强降低。若按图2所示连接装置,进行实验II,则会观察到c中长导管口有气泡产生,原因是b中HCl气体溶于水,导致瓶内压强低于大气压,使瓶外空气进入c中。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】根据下表回答相关问题。
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度(g/100g水) | KNO3 | 13.3 | 31.6 | 63.9 | 110.0 | 169.0 | 246.0 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
①表中两种物质的溶解度相等的温度范围是在___________℃。
②20℃时,硝酸钾的溶解度是31.6 g/100g水,其含义是___________。该温度下,将20gKNO3
放入50g水中,充分搅拌,所得溶液的质量是_______g。要进一步提高该溶液的溶质质量分数,可进行的操作是__________。
③硝酸钾溶液中含有少量氯化钠杂质,提纯的方法是_________ 。
④60℃时,对100g硝酸钾饱和溶液(如A烧杯)进行如下操作,请回答相关问题:
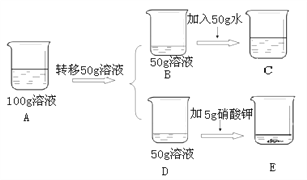
上述溶液中所含溶质的质量D_____E(填“>”或“<”或“=”,下同),溶液不饱和的是___(用A、B、C、D、E填空),溶液B、C、E中溶质质量分数的大小关系是__________。