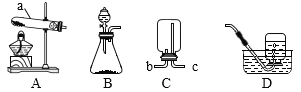
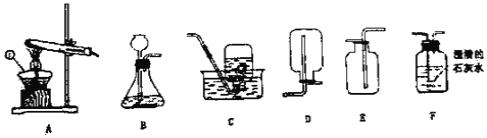
题目内容
【题目】“双吸剂”是一种常见袋装食品的保鲜剂,能吸收空气中的氧气、二氧化碳、水蒸气等。化学兴趣小组的同学在某食品袋中发现一包“双吸剂”,其标签如图所示。同学们对这包久置的“双吸剂”固体样品很好奇,设计实验进行探究。

(提出问题)久置“双吸剂”固体的成分是什么?
(查阅资料)
铁与氯化铁溶液在常温下发生反应生成氯化亚铁:Fe+2FeCl3═3FeCl2。
(作出猜想)久置固体中一定有活性炭可能含有及________________。
(实验探究)下表是小组同学设计的实验方案和记录的实验报告,请你补充完整:
实验操作 | 实验现象 | 实验结论 |
①取3g固体样品仔细观察,用磁铁吸固体,置于烧杯中,加20 mL水,用温度计测量溶解前后液体温度,过滤,所得滤液备用。 | 固体样品中有黑色粉末, 较多白色固体及少量红棕色固体,少量黑色粉末可以被磁 铁吸引,温度计温度无明显变化,得到无色滤液 | 样品中____________ |
②取少量①中无色滤液,滴加无色酚酞。 | 溶液有无色变为红色 | 样品中一定含Ca(OH)2 |
③取少量固体样品放入试管 中,加适量的试剂Y,用带导管的单孔橡皮塞塞紧试管口,导管另一端伸入澄清石灰水中。 | 试管中固体逐渐减少,有大量无色气体产生,得到浅绿色溶液,有少量黑色固体不溶,澄清的石灰水变浑浊。 | 样品中含有活性炭、CaCO3 |
(实验释疑)确定了久置“双吸剂”固体的成分后,几位同学又提出了以下问题:
Ⅰ步骤③中加入试剂 Y 后,溶液却不呈黄色的原因是_______________。
Ⅱ查阅资料得知,铁粉作脱氧剂时,为了达到更好的脱氧效果,会向其中加入少量的氯化钠。请设计实验说明氯化钠存在时铁粉脱氧效果更好:__________________。
【答案】Fe、Fe2O3、CaO、Ca(OH)2和CaCO3 Fe、Fe2O3 Fe2O3+6HCl═2FeCl3+3H2O,Fe+2FeCl3=3FeCl2 分别取相同的两个铁钉,一个放入普通水中,一个放置在食盐水中,食盐水中的铁钉锈蚀更快
【解析】
解:[作出猜想]铁生锈水生成氧化铁,铁可能部分变质,可能全部变质,氧化钙和水反应生成氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙沉淀,所以久置固体中一定有活性炭可能含有及:Fe、Fe2O3、CaO、Ca(OH)2和CaCO3;
[实验探究]固体样品中有黑色粉末, 较多白色固体及少量红棕色固体,少量黑色粉末可以被磁 铁吸引,温度计温度无明显变化,得到无色滤液;可知含有Fe、Fe2O3;
[实验释疑]I、氧化铁和盐酸反应生成氯化铁和水,氯化铁和铁反应生成氯化亚铁,所以步骤③中加入试剂Y后,溶液呈不呈黄色的原因是:Fe2O3+6HCl═2FeCl3+3H2O,Fe+2FeCl3=3FeCl2;
II、设计实验说明氯化钠存在时,铁粉脱氧效果更好的操作是:分别取相同的两个铁钉,一个放入普通水中,一个放置在食盐水中,食盐水中的铁钉锈蚀更快。

【题目】图表法是一种常用的数据处理方法,也是化学学习的重要工具。请结合所给图表回答问题。
(1)图a是硝酸钾和氯化钾的溶解度曲线。25℃将等质量的氯化钾和硝酸钾分别加入到各盛有 100g 水的两个烧杯中,充分搅拌后得无色溶液,降温至 15℃时 出现如图 b 所示现象。烧杯甲中溶解的溶质是________________________(填化学式)。 硝酸钾中含有少量氯化钾,应采用____________的方法提纯硝酸钾。
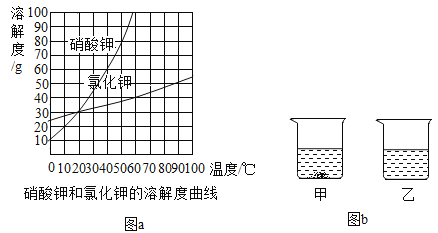
(2)如图数轴中 A、B、C 处表示的是常温时将氯化钠、硝酸铵、烧碱三种物质 分别溶于 100g 水所得溶液的温度,其中表示硝酸铵的是__________填序号)。

(3)如图是氢氧化钠和碳酸钠在不同温度不同溶剂中的溶解度表。
溶质 溶解度 溶剂 | 氢氧化钠 | 碳酸钠 | ||
20℃ | 40℃ | 20℃ | 40℃ | |
水 | 109g | 129g | 21.8g | 49g |
酒精 | 17.3g | 40g | 不溶 | 不溶 |
20℃时,若将 0.8g 氢氧化钠分别投5g 酒精的大试管中,振荡,再向 其中通入 CO2,观察到的实验现象为__________________,反应方程式为__________________________。