题目内容
 石头纸是一种介于纸张和塑料之间的新型材料.石头纸的主要成分是碳酸钙,为测定某厂生产的石头纸中碳酸钙的质量分数,称取10g石头纸样品,剪碎后加入40g稀硫酸恰好完全反应(假设石头纸中的其他成分不溶于水,也不与稀盐酸反应),测得有关数据如图所示.请计算:
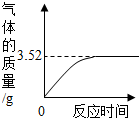
石头纸是一种介于纸张和塑料之间的新型材料.石头纸的主要成分是碳酸钙,为测定某厂生产的石头纸中碳酸钙的质量分数,称取10g石头纸样品,剪碎后加入40g稀硫酸恰好完全反应(假设石头纸中的其他成分不溶于水,也不与稀盐酸反应),测得有关数据如图所示.请计算:(1)样品中碳酸钙完全反应时产生二氧化碳的质量为
(2)该厂生产的石头纸中碳酸钙的质量分数(写出计算过程);
(3)实验中所使用的稀盐酸的溶质质量分数为
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)分析图中数据,判断碳酸钙完全反应时所放出二氧化碳的质量,
(2)根据反应的化学方程式,由此时生成二氧化碳的质量计算出样品中所含碳酸钙的质量.
(3)分析数据判断盐酸完全反应与生成二氧化碳之间的质量关系,由二氧化碳的质量求出盐酸的溶质质量分数.
(2)根据反应的化学方程式,由此时生成二氧化碳的质量计算出样品中所含碳酸钙的质量.
(3)分析数据判断盐酸完全反应与生成二氧化碳之间的质量关系,由二氧化碳的质量求出盐酸的溶质质量分数.
解答:解:(1)分析图中数据,盐酸与碳酸钙反应时生成二氧化碳的质量是3.52g; 故填:3.52;
设,碳酸钙的质量分数为x,盐酸的溶质质量分数为y
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 73 44
10gx 40gy 3.52g
=
,
=
x=80% y=14.6%
答:(2)“石头纸”样品中CaCO3的质量分数为80%.
(3)稀盐酸的溶质质量分数为14.6%
故答案为:(2)80% (3)14.6%.
设,碳酸钙的质量分数为x,盐酸的溶质质量分数为y
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 73 44
10gx 40gy 3.52g
| 100 |
| 10gx |
| 44 |
| 3.52g |
| 73 |
| 40gy |
| 44 |
| 3.52g |
x=80% y=14.6%
答:(2)“石头纸”样品中CaCO3的质量分数为80%.
(3)稀盐酸的溶质质量分数为14.6%
故答案为:(2)80% (3)14.6%.
点评:根据图中数据中随稀盐酸质量变化生成二氧化碳气体的质量变化情况的分析,可对反应的情况有明确的判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
滴有酚酞的Ba(OH)2溶液与下列各物质恰好完全反应后,溶液仍为红色的是( )
| A、HCl |
| B、HNO3 |
| C、CO2 |
| D、Na2SO4 |
 (1)如表列出了氯化铵在不同温度下的溶解度.
(1)如表列出了氯化铵在不同温度下的溶解度.