题目内容
【题目】以下是今年我市实验操作考察的内容,请回答相关问题.
(1)【实验目的】证明氢氧化钠溶液与稀盐酸发生了反应且生成了新物质; 【实验原理】(用化学方程式表示);
(2)【药品仪器】 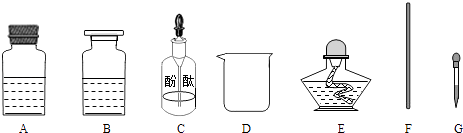
【实验步骤】
①取(选填“A”或“B”)中试剂加入至D中,滴加2滴酚酞试液,溶液呈红色;
②用(填仪器名称)向①中溶液滴加稀盐酸,直至红色消失;
③向②中溶液继续滴加过量稀盐酸,溶液保持无色;
④用F蘸取③中溶液,在酒精灯上灼烧,有白色固体产生.
(3)【思考拓展】 ①步骤③的目的是:;
②如不使用酸碱指示剂,进一步确认步骤④中的白色固体不是氢氧化钠的方法是:;
(4)已知酚酞试液在不同pH时的变色情况如下表.某同学发现:向某氢氧化钠溶液中滴加酚酞试液后,溶液显无色;逐滴滴加稀盐酸,溶液先变红,后褪至无色.你认为该氢氧化钠溶液滴加酚酞试液显无色的原因可能是: . 请设计实验证明你的猜想(写出简要的操作步骤与现象: .
pH | <8.2 | 8.2~10.0 | >10.0 |
颜色 | 无色 | 红色 | 无色 |
【答案】
(1)HCl+NaOH═NaCl+H2O
(2)A;胶头滴管
(3)充分反应掉所有的氢氧化钠;取少量水将其溶解,观察温度的变化
(4)浓度过大;取少量的浓氢氧化钠于烧杯中,向其中滴入酚酞试液,如果颜色为无色,然后用水稀释,再滴入酚酞试液,颜色变为红色,则证明猜想正确
【解析】解:【实验原理】:盐酸和氢氧化钠溶液混合发生的是中和反应生成物为氯化钠和水,其化学方程式为:HCl+NaOH═NaCl+H2O.【实验步骤】①因为盛放碱溶液的瓶盖不能是玻璃的,故A瓶盛的是氢氧化钠溶液,B瓶盛的是盐酸,又因为酚酞的变色是遇酸无色,遇碱变红色,故取A中试剂加入至D中,滴加2滴酚酞试液,溶液呈红色. ②用胶头滴管滴加盐酸,所以答案是胶头滴管;
【思考拓展】(1)步骤③的目的是,充分反应掉所有的氢氧化钠.(2)因为氢氧化钠在溶解时放热,而氯化钠在溶解时没有温度的变化,故可取少量水将其溶解,观察温度的变化.(3)由酚酞试液在不同pH时的变色情况可知,该氢氧化钠溶液滴加酚酞试液显无色的原因可能是浓度过大;
为了证明这个猜想,我们可以取少量的浓氢氧化钠于烧杯中,向其中滴入酚酞试液,如果颜色为无色,然后用水稀释,再滴入酚酞试液,颜色变为红色,则证明猜想正确;
所以答案是:【实验原理】:HCl+NaOH═NaCl+H2O;【实验步骤】①A;②胶头滴管;【思考拓展】(1)充分反应掉所有的氢氧化钠;(2)取少量水将其溶解,观察温度的变化;(3)浓度过大;取少量的浓氢氧化钠于烧杯中,向其中滴入酚酞试液,如果颜色为无色,然后用水稀释,再滴入酚酞试液,颜色变为红色,则证明猜想正确;
【考点精析】根据题目的已知条件,利用中和反应及其应用的相关知识可以得到问题的答案,需要掌握中和反应:酸与碱作用生成盐和水的反应.

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案【题目】下列鉴别物质的方法不可行的是
选项 | 被鉴别的物质 | 鉴别方法 |
A | CH4和H2 | 点燃后产生的气体分别通入澄清石灰水 |
B | Na2CO3溶液和NaCl溶液 | 分别滴加稀盐酸 |
C | NaOH溶液和Ca(OH)2溶液 | 分别滴加石蕊试液 |
D | Ca(OH)2溶液和稀H2SO4 | 分别滴加酚酞试液 |