题目内容
【题目】中国探测卫星“嫦娥二号”2010年10月1日在西昌卫星发射中心成功发射。长三丙运载火箭将嫦娥二号送入奔月轨道,飞行时间仅需112小时。
(1)长三丙运载火箭的第一、二级燃料采用偏二甲肼和四氧化二氮作常规推进剂,当完全反应的化学方程式为X+2N2O4 = 3N2+2CO2+4H2O,则目前国际最普遍使用的火箭燃料偏二甲肼的化学式为______。
(2)发射前经过近10小时加注100吨燃烧剂和氧化剂,四氧化二氮是一种具有强腐蚀的有毒气体,其化学式为____,其中氮元素化合价为____。常温下容易转变成二氧化氮,将发生_____(“物理”“化学”)变化。在加注火箭燃料时应该采取的安全保护措施是_______。
(3)我国长三丙运载火箭第三级采用燃料是液氢、助燃剂是液氧的火箭发动机,成为世界上第三个掌握控制液态氢技术的国家。氧气从淡蓝色液体变成无色气体发生了_____变化,氢气燃烧的化学方程式为___________。液态氢作燃料除燃烧时产生较大的推动力外,另一个优点是_____________。但目前大量应用氢能的困难是(写一个)__________。
【答案】C2H8N2 N2O4 +4 化学 使用防毒面具和防护服、用水稀释、防静电和雷电等 物理 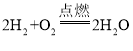 污染少 制取氢气成本高和储存困难
污染少 制取氢气成本高和储存困难
【解析】
(1)根据质量守恒定律结合化学方程式X+2N2O4 = 3N2+2CO2+4H2O,反应前4个N原子、8个O原子,反应后6个N原子、2个C原子、8个H原子、8个O原子,可知每个X分子中含2个C原子,8个H原子,2个N原子,则偏二甲肼的化学式为C2H8N2。
(2)四氧化二氮的化学式为N2O4,氧元素化合价为-2,根据化合物中化合价代数和为零的原则,可知氮元素化合价为+4。常温下容易转变成二氧化氮,有新物质生成,属于化学变化。根据四氧化二氮的性质:强腐蚀、有毒气体、常温下容易转变成二氧化氮,在加注火箭燃料时应该采取的安全保护措施是使用防毒面具和防护服、用水稀释、防静电和雷电等。
(3)氧气从淡蓝色液体变成无色气体,只是状态发生了变化,没有新物质生成,属于物理变化,氢气燃烧生成水,反应的化学方程式为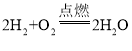 。液态氢作燃料除燃烧时产生较大的推动力外,另一个优点是只有水生成,污染少。目前大量应用氢能的困难是制取氢气成本高和储存困难。
。液态氢作燃料除燃烧时产生较大的推动力外,另一个优点是只有水生成,污染少。目前大量应用氢能的困难是制取氢气成本高和储存困难。

 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案【题目】某兴趣小组在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液逐滴加入稀硫酸,一会儿发现忘记了滴加指示剂。此时,他们停止滴加稀硫酸,并对烧杯内溶液中的溶质成分进行探究。
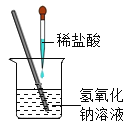
(1)写出该中和反应的化学方程式为______________;
(2)探究烧杯内溶液中溶质的成分:
(提出问题)该烧杯内溶液中的溶质是什么?
(猜想)猜想一:溶质有硫酸钠和氢氧化钠;猜想二:溶质只有硫酸钠;猜想三:_________;
(进行实验)
实验步骤 | 可能观察到的现象 | 结 论 |
①取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡; | _______________ | 猜想一不正确 |
②再取少量烧杯内溶液于另一支试管中,逐滴加入_____溶液至过量 | ______________ | 猜想二不正确,猜想三正确。 |
(反思与拓展)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑__________;