题目内容
【题目】圆规是学生学习常使用的工具,在圆规组成的材料中:
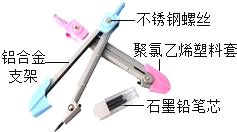
(1)属于有机合成材料的是_____,属于合金的是_____(选一种材料名称).
(2)使用石墨作图的优点:_____.
(3)能证明铝比铜活泼的化学方程式:_____.
(4)上一世纪50年代,霍尔等人以熔融的FeS作溶剂,在一定的高温、高压条件下使石墨第一次转化为金刚石,其反应:C(石墨)→C(金刚石).石墨转化为金刚石属于_____变化(化学、物理).
【答案】聚氯乙烯塑料套 铝合金支架 石墨稳定画能长久保存,且石墨有滑腻感,作图流畅,清晰,错易修改等 2Al+3CuSO4═3Cu+Al2(SO4)3 化学
【解析】
根据已有的材料的类别、石墨的性质以及化学方程式的书写的知识进行分析解答即可。
(1)据图可以看出,聚氯乙烯塑料套属于有机合成材料,铝合金支架、不锈钢螺丝属于金属材料,故填:聚氯乙烯塑料套,铝合金支架
(2)石墨的主要成分是碳,在常温下化学性质很稳定,且石墨是自然界中最软的矿物之一,故填:石墨稳定画能长久保存,且石墨有滑腻感,作图流畅,清晰,错易修改等
(3)铝能与硫酸铜反应生成铜和硫酸铝,故填:2Al+3CuSO4═3Cu+Al2(SO4)3
(4)石墨转化为金刚石是生成了新的物质,属于化学变化,故填:化学

 春雨教育同步作文系列答案
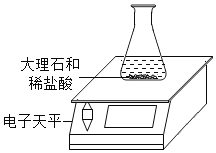
春雨教育同步作文系列答案【题目】某同学对“影响稀盐酸和大理石反应快慢的因素”进行探究.选取的药品:成分相同的粉末状大理石、块状大理石两种样品;浓度为16%、9%的稀盐酸.采用控制变量法设计实验方案,以5分钟内收集到CO2的质量作为判断依据.已知稀盐酸足量且样品中杂质不与稀盐酸反应,实验装置如图.读取电子天平的示数,据此计算生成的CO2的质量,记录的数据如表
实验序号 | 大理石 (各6g) | 稀盐酸的浓度 | 反应开始到5分钟产生CO2的质量 | 反应结束产生的CO2的质量 |
① | 块状 | 16% | 2.16g | 2.2g |
② | 块状 | 9% | 1.42g | 2.2g |
③ | 粉末 | 16% | 2.33g | 2.2g |
④ | 粉末 | 9% | 1.93g | m2 |
(1)稀盐酸的浓度对该反应快慢的影响:_____.
(2)实验过程中,通过观察如图装置中的哪一现象可判断反应结束_____.
(3)结合表格分析,实验④反应结束后m2的值_____.
(4)探究大理石的颗粒大小对该反应快慢的影响,其实验序号分别是_____.
(5)计算该大理石(6g)样品中含碳酸钙的质量为_____.
【题目】“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;
b.可能与锌的形状有关。
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
实验 编号 | 硫酸的质量 分数(均取 20 mL) | 锌的形状 (均取1 g) | 氢气的体积(mL) (均收集3分钟) |
① | 20% | 锌粒 | 31.7 |
② | 20% | 锌片 | 50.9 |
③ | 30% | 锌粒 | 61.7 |
④ | 30% | 锌片 | 79.9 |
(1)写出稀硫酸与锌反应的化学方程式:________________________。
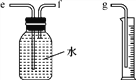
(2)小兵用如图所示装置收集并测量氢气的体积,其中量筒的作用是________________________________________,氢气应从________(填“e”“f”或“g”)管通入。
【收集证据】(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是____________。
【得出结论】(4)结论是________________________________________________________________。
(5)下表是小兵第①组实验的详细数据。
时段(均 为1分钟) | 第1 分钟 | 第2 分钟 | 第3 分钟 | 第4 分钟 | 第5 分钟 | 第6 分钟 |
H2的体积 | 3.1 mL | 16.7 mL | 11.9 mL | 9.6 mL | 7.6 mL | 6.0 mL |
请描述锌与硫酸反应的快慢的变化并解释原因:______________________________。
(6)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证。___________________。
【题目】下面是甲、乙实验小组完成的相关实验。
甲小组:利用下图装置研究燃烧条件(已知白磷的着火点为40℃)。
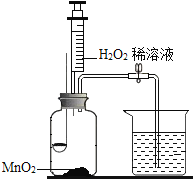
步骤Ⅰ:烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞。
步骤Ⅱ:用注射器向瓶内推入适量H2O2 溶液
(1)H2O2稀溶液与MnO2接触时发生反应的文字表达式为_____;
(2)实验中,推入H2O2溶液前,燃烧匙中的白磷不燃烧,原因是_____;推入H2O2溶液后,观察到烧杯中的现象是_____。
乙小组:哪些因素影响过氧化氢分解的速率?
实验序号 | H2O2溶 液浓度% | H2O2溶液体积/mL | 温度℃ | MnO2的用量/g | 收集氧气的体积/mL | 反应所需 的时间/s |
① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
③ | 30 | 5 | 35 | 2 | 49.21 | |
④ | 30 | 5 | 55 | 2 | 10.76 |
(1)通过实验对比可知,化学反应速率与浓度和温度有关系。
(2)化学反应的实质是微观粒子相互接触、碰撞的结果,化学反应速率与微观粒子相互接触、碰撞的概率有关。试从微观角度解释“反应物浓度越大,化学反应速率越快”的原因是:_____;
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量_____(填“减小”或“不变”或“增大”)。