题目内容
【题目】某校实验小组的同学用木炭与氧化铜反应,证明木炭具有还原性.实验装置图如下:
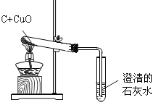
请填写实验报告.
(1)实验用品:
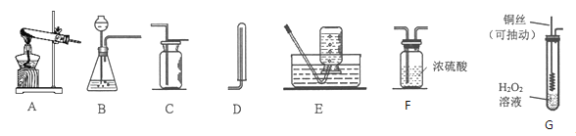
仪器:________.
药品:木炭、氧化铜、澄清石灰水
(2)
现象 | 分析 |
_______ | _______ |
_______ | _______ |
(3)结论
结论:________,反应的化学方程式为:________.
(4)问题和分析
问题:在加热一段时间后,装有木炭和氧化铜试管口部,凝聚了少量的水.但是反应物中并没有氢元素,为什么会有水产生呢?我的________________.
【答案】酒精灯、铁架台、试管、带橡胶塞的导管澄清石灰水由澄清逐渐变浑浊(或澄清石灰水由澄清逐渐变浑浊,又逐渐变澄清)木炭得到了氧化铜中的氧,生成了二氧化碳,二氧化碳使澄清石灰水逐渐变浑浊试管中(有一部分)黑色粉末逐渐变红色 氧化铜失去氧而变成单质铜,单质铜的颜色为红色炭是使氧化铜还原为铜的物质(或木炭夺去氧化铜里的氧)C+2CuO ![]() 2Cu+CO2↑反应物是木炭和氧化铜,并没有氢元素参加化学反应.根据质量守恒定律,在木炭和氧化铜发生化学反应的过程中,不可能有水生成.但在加热一段时间后,试管口部,凝聚了少量的水,说明反应物木炭和氧化铜吸收水分,加热过程中水分蒸发出来,在试管口部冷凝
2Cu+CO2↑反应物是木炭和氧化铜,并没有氢元素参加化学反应.根据质量守恒定律,在木炭和氧化铜发生化学反应的过程中,不可能有水生成.但在加热一段时间后,试管口部,凝聚了少量的水,说明反应物木炭和氧化铜吸收水分,加热过程中水分蒸发出来,在试管口部冷凝
【解析】
1.考查对常见仪器的辨别和认识,用到的仪器有:酒精灯、铁架台、试管、带橡胶塞的导管;2.加热的试管内发生的反应为:2CuO+C![]() 2Cu+CO2
2Cu+CO2![]() ,所以现象为:试管内黑色粉末逐渐变为红色,是因为氧化铜失去氧而变成单质铜,单质铜的颜色为红色;盛澄清石灰水的试管内发生的反应为CO2+Ca(OH)2=CaCO3↓+H2O,是因为木炭得到了氧化铜中的氧,生成了二氧化碳,二氧化碳使澄清石灰水逐渐变浑浊;3.通过上面对现象的分析可知氧化铜失去了氧变为铜,碳得到了氧化铜中的氧变为了二氧化碳,所以可以得出结论:是碳夺去了氧化铜中的氧;书写化学方程式必须注意反应条件、气体符号、配平,确保方程式书写完整才能得分,2CuO+C
,所以现象为:试管内黑色粉末逐渐变为红色,是因为氧化铜失去氧而变成单质铜,单质铜的颜色为红色;盛澄清石灰水的试管内发生的反应为CO2+Ca(OH)2=CaCO3↓+H2O,是因为木炭得到了氧化铜中的氧,生成了二氧化碳,二氧化碳使澄清石灰水逐渐变浑浊;3.通过上面对现象的分析可知氧化铜失去了氧变为铜,碳得到了氧化铜中的氧变为了二氧化碳,所以可以得出结论:是碳夺去了氧化铜中的氧;书写化学方程式必须注意反应条件、气体符号、配平,确保方程式书写完整才能得分,2CuO+C![]() 2Cu+CO2
2Cu+CO2![]() ;4.反应体系中的水有两个可能来源:一是反应生成的水,二是反应物带入的水;首先分析第一种情况:因为反应物是木炭和氧化铜,并没有氢元素参加化学反应.根据质量守恒定律,在木炭和氧化铜发生化学反应的过程中,不可能有水生成;第二种情况:根据实验记录是在实验进行了一段时间试管口才有水凝聚,说明是反应前反应物受潮或吸收了水,加热后水分蒸发出来了,在试管口遇冷凝聚。
;4.反应体系中的水有两个可能来源:一是反应生成的水,二是反应物带入的水;首先分析第一种情况:因为反应物是木炭和氧化铜,并没有氢元素参加化学反应.根据质量守恒定律,在木炭和氧化铜发生化学反应的过程中,不可能有水生成;第二种情况:根据实验记录是在实验进行了一段时间试管口才有水凝聚,说明是反应前反应物受潮或吸收了水,加热后水分蒸发出来了,在试管口遇冷凝聚。