题目内容
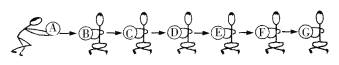
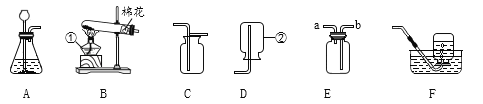
【题目】根据下列装置图,回答有关问题:
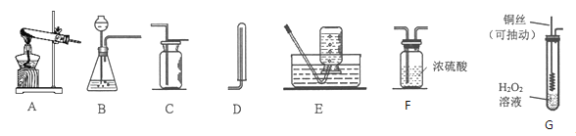
(1)实验室用装置A和E制取氧气,其反应的化学方程式为__________________。当观察到______________时才开始收集。
(2)实验室用过氧化氢制取氧气的化学方程式为______,若要制取并收集一瓶干燥的氧气,应选用装置的连接顺序为______(选填字母)。
(3)实验改进:查阅资料发现,氧化铜可以用作过氧化氢分解制氧气的催化剂.现有一根洁净的铜丝,实验前先将其绕成螺旋状,再经过______处理.改进后的发生装置如图G所示(己略去夹持装置)。
①铜丝绕成螺旋状的作用是______;
A.收集到更多的02 B.加快反应速率 C.没有影响
②与装置B比较,改进后装置的优点是______。
【答案】2KMnO4![]() K2MnO4+MnO2+O2↑导管口处气泡连续均匀放出2H2O2
K2MnO4+MnO2+O2↑导管口处气泡连续均匀放出2H2O2![]() 2H2O+O2↑B、F、C灼烧B可随时控制反应的发生和停止
2H2O+O2↑B、F、C灼烧B可随时控制反应的发生和停止
【解析】
(1)装置A适用于固体加热制取氧气,因为试管口有棉花团,所以是加热高锰酸钾制取氧气,同时生成锰酸钾和二氧化锰,反应的化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;当用排水法收集氧气时,导管口刚开始排出的装置内的空气,应等到导管口处气泡连续均匀放出时才能收集;
K2MnO4+MnO2+O2↑;当用排水法收集氧气时,导管口刚开始排出的装置内的空气,应等到导管口处气泡连续均匀放出时才能收集;
(2)过氧化氢在二氧化锰的催化作用下分解为水和氧气,反应的化学方程式为:2H2O2![]() 2H2O+O2↑;该反应属于固液常温型,所以选择装置来制取,用盛有浓硫酸的装置F来进行干燥,最后用向上排空气法来收集干燥的氧气;(3)将铜丝灼烧,铜与氧气反应生成氧化铜;
2H2O+O2↑;该反应属于固液常温型,所以选择装置来制取,用盛有浓硫酸的装置F来进行干燥,最后用向上排空气法来收集干燥的氧气;(3)将铜丝灼烧,铜与氧气反应生成氧化铜;
①将铜丝绕成螺旋状,增大了与反应物的接触面积,加快了反应的速率;
②改进后的装置,通过抽动铜丝来控制反应的发生和停止。

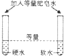
【题目】某校实验小组的同学用木炭与氧化铜反应,证明木炭具有还原性.实验装置图如下:
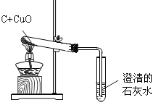
请填写实验报告.
(1)实验用品:
仪器:________.
药品:木炭、氧化铜、澄清石灰水
(2)
现象 | 分析 |
_______ | _______ |
_______ | _______ |
(3)结论
结论:________,反应的化学方程式为:________.
(4)问题和分析
问题:在加热一段时间后,装有木炭和氧化铜试管口部,凝聚了少量的水.但是反应物中并没有氢元素,为什么会有水产生呢?我的________________.
【题目】现有一瓶标签破损的白色固体(如图),化学兴趣小组的同学们决定对该白色固体成分进行实验探究。
![]()
(提出问题)这瓶白色固体的成分是什么?
(查阅资料)氯化钠、硫酸钠、硝酸钠的溶液显中性。
(作出猜想)猜想1:氯化钠;猜想2:氢氧化钠;猜想3:碳酸钠;猜想4:……
(实验探究)为了证明猜想,同学们取白色固体置于烧杯中,加水配成溶液,进行如下实验探究:
序号 | 实验步骤 | 实验现象 | 实验结论 |
1 | 取少量溶液于试管中,滴加酚酞溶液 | 酚酞溶液变红 | 说明溶液显________性,猜想1不成立 |
2 | 取少量溶液于试管中,滴加稀盐酸 | 有气泡生成,气体通入澄清石灰水,石灰水变浑浊 | 猜想2_________(填“成立”或“不成立”) |
3 | 取少量溶液于试管中,滴加氯化钙溶液 | 试管中______________________________________ | 猜想3不成立 |
(讨论交流)实验后,同学们找老师交流探讨,请教之后得出白色固体是____________________。
(拓展)为了进一步证实结论,同学们在老师的指导下,又做了该物质受热分解的实验,确定结论正确。