题目内容
【题目】学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能否起到类似MnO2的催化作用呢?于是进行了以下探究。
(猜想)Ⅰ.CuO不是催化剂,也不参加反应,反应前后质量和化学性质不变;
Ⅱ. CuO参与反应生成O2,反应前后质量和化学性质发生改变;
Ⅲ. CuO是反应的催化剂,反应前后_________________。
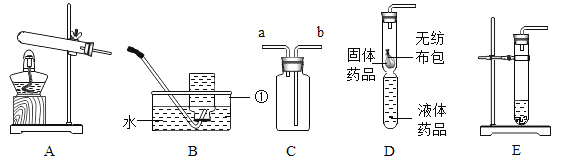
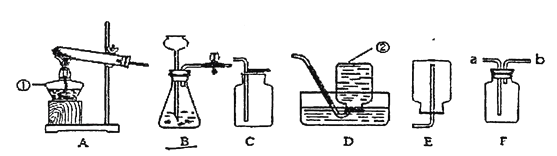
(实验及结论)用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
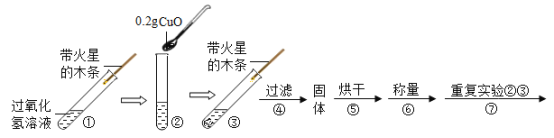
(1)填写下表:
步骤③现象 | 步骤⑥ | 步骤⑦现象 | 结论 |
溶液中有气泡冒出,带火星木条复燃 | 称量所得固体质量为 ____________g | 溶液中有气泡冒出,_____________ | 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立。 |
(表达与交流)过氧化氢被CuO催化分解放出氧气的化学反应方程式为_____________。
(反思与拓展)
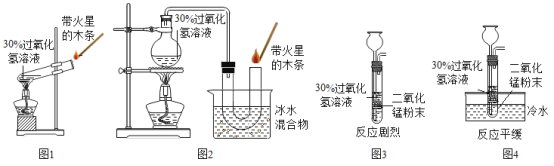
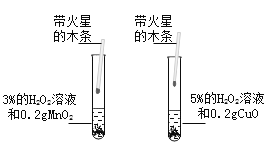
(1)甲同学为研究催化剂种类对催化效果的影响,用等量的两份过氧化氢溶液设计了以下实验,大家认为该方案不可行,其原因是_________。
(2)以下有关催化剂的说法正确的是_____________(填序号)。
①二氧化锰是催化剂
②某些化学反应可以有多个催化剂
③一种物质可能作为多个反应的催化剂
④所有化学反应都需要催化剂
⑤催化剂只能加快化学反应速率
【答案】质量和化学性质不变 0.2 带火星的木条复燃 2H2O2![]() 2H2O+O2↑ 实验中除了催化剂种类不同,过氧化氢溶液的溶质质量分数也不同,无法形成对照 ②③
2H2O+O2↑ 实验中除了催化剂种类不同,过氧化氢溶液的溶质质量分数也不同,无法形成对照 ②③
【解析】
[猜想]如果CuO是反应的催化剂,反应前后质量和化学性质不变;
[实验及结论]氧化铜对过氧化氢的分解有催化作用,能加快其分解速率生成氧气的速率,故现象是有气泡,带火星的木条复燃;催化剂的特点是“一变,两不变”,反应前后其质量不变,氧化铜的质量仍为0.2g;催化剂的特点是“一变,两不变”,其中反应速率改变,这里是加快,所以现象是溶液中有气泡放出,带火星的木条复燃。
[表达与交流]过氧化氢在氧化铜的催化作用下分解生成水和氧气,化学方程式为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
[反思与拓展](1)甲同学为研究催化剂种类对催化效果的影响,所以实验的变量为催化剂种类,图二实验中过氧化氢溶液的溶质质量分数不同,无法形成对照;
(2)①二氧化锰不一定是催化剂,其它物质也可以作催化剂,同时二氧化锰在高锰酸钾分解的反应中是生成物,不是催化剂,故说法错误。
②某些化学反应可以有多个催化剂,如过氧化氢分解的反应中,二氧化锰、氧化铜、硫酸铜溶液等均可以作催化剂,故说法正确。
③一种物质可以催化多个化学反应,二氧化锰可以作氯酸钾、过氧化氢溶液分解的催化剂,故说法正确。
④不是所有化学变化都需要催化剂,如人的呼吸作用,故说法错误。
⑤催化剂既能加快,也能减慢化学反应速率,故说法错误。
故②③说法正确。
故答案为:[猜想]质量和化学性质不变;
[实验及结论]0.2;带火星的木条复燃;
[表达与交流]2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
[反思与拓展](1)实验中除了催化剂种类不同,过氧化氢溶液的溶质质量分数也不同,无法形成对照;
(2)②③。

 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案【题目】3.0g某物质完全燃烧后生成4.4gCO2和1.8g水.则对该物质相关判断正确的是( )
| A. | 该物质只含碳、氢元素 |
| B. | 该物质一定含有碳、氢元素,可能含有氧元素 |
| C. | 该物质由碳、氢、氧元素组成 |
| D. | 该物质分子中碳原子和氢原子的个数比为1:1 |