题目内容
【题目】把8.9gMg、Zn合金放入一定量的稀盐酸中,恰好完全反应,产生0.4g H2,在上述反应后的溶液中滴入足量的NaOH溶液,充分反应后生成NaCl的质量为( )
A. 23.4g B. 29.25g C. 30.5g D. 26.25g
【答案】A
【解析】
镁、锌和稀盐酸反应生成氢气、氯化镁、氯化锌,氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,和氯化锌反应生成氢氧化锌沉淀和氯化钠,稀盐酸中的氯离子完全转化成氯化钠中的氯离子。
由Mg+2HCl═MgCl2+H2↑,Zn+2HCl═ZnCl2+H2↑可知,2Cl-~H2↑,
设氯离子质量为x,
2Cl-~H2↑,
71 2
x 0.4g
![]()
x=14.2g,
充分反应后生成NaCl的质量为![]() 。故选A。
。故选A。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案 智趣寒假作业云南科技出版社系列答案
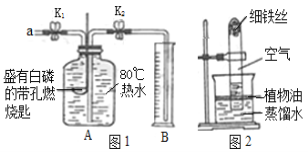
智趣寒假作业云南科技出版社系列答案【题目】某同学进行如下图的两个实验。
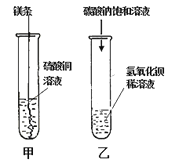
(l)甲实验观察到的现象是________________,溶液由蓝色变成无色。
(2)乙实验中反应的化学方程式为___________;
(3)把甲、乙反应后的溶液倒入同一烧怀,发现有白色沉淀生成。他决定对白色沉淀的成分进行探究。
(查阅资料)硫酸钡不溶于酸。
(提出猜想)白色沉淀为:Ⅰ.________Ⅱ.Mg(OH)和BaSO4;Ⅲ. Mg(OH)2和MgCO3.
(实验方案)
实验操作 | 实验现象与结论 |
过滤、洗涤白色沉淀备用;向白色沉淀中加入盐酸至过量 | ①沉淀全部溶解,且无其它现象;猜想Ⅰ成立;其化 学反应方程式为 ________________________。 ②若_________________且无气体产生,猜想Ⅱ成立。 ③若沉淀完全溶解,_______________,猜想Ⅲ成立。 |
(拓展与思考)如果猜想Ⅲ成立,产生此结果的原因是做乙实验时______________;
上述白色沉淀的成分不可能出现的组合是Mg(OH)2、MgCO3和BaSO4,原因是________________。