题目内容
【题目】某化学兴趣小组欲探究实验室的一包白色固体( 已知含碳酸钠)的具体成分 。
他们猜测可能含有硝酸钡、硫酸钠、氢氧化钠中的一种或几种。 通过查阅资料发现硝酸钡溶于水呈中性,硫酸钠溶于水呈弱碱性。以下是实验步骤:
步骤一:取少量白色固体于烧杯中.向烧杯中加入足量水并不断搅拌,固体部分溶解。
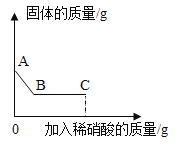
步骤二:接着向烧杯中加入足量稀硝酸并不断搅拌,测定固体质量变化,并画出如图所示图象。
(1)步骤一的实验目的是_______________________________________;
(2)步骤二中他们观察到的现象是_____________________________;综合步骤一、步骤二能确定该白色粉末中一定含有_____________________________。
(3)若要继续确定该白色粉末的成分,请你设计实验方案:
实验操作 | 预期实验现象 | 实验结论 |
____ | _____ | ____ |
【答案】检验固体中是否有硝酸钡 沉淀部分溶解,有气泡产生 硝酸钡、硫酸钠 取步骤一所得溶液,先加入足量硝酸钡溶液,再向上层清液中滴加几滴酚酞试液 酚酞试液变红 白色固体中还含有氢氧化钠
【解析】
(1)步骤一取少量白色固体溶于水,实验目的是通过观察是否产生沉淀来检验固体中是否有硝酸钡;
(2)步骤二向烧杯中加入足量稀硝酸,依据图象固体变化曲线,沉淀部分溶解,说明固体中既有碳酸钡也有硫酸钡,则观察到的现象是沉淀部分溶解,有气泡产生;有碳酸钡产生,则固体中含有硝酸钡;有硫酸钡产生,则固体中含有硫酸钠,故可确定该白色粉末中一定含有硝酸钡、硫酸钠。
(3)要继续确定该白色粉末的成分,就是要确定是否含有氢氧化钠。实验方案是: 取步骤一所得溶液,先加入足量硝酸钡溶液,再向上层清液中滴加几滴酚酞试液;如果观察到酚酞试液变红,则白色固体中还含有氢氧化钠。

 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案【题目】下列图象中有关的量的变化与对应叙述相符的是( )
A | B | C | D |
|
|
|
|
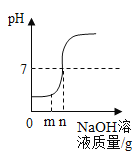
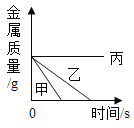
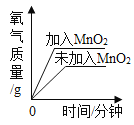
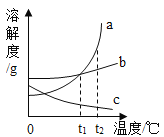
向盐酸中加入的氢氧化钠溶液为mg时,所得溶液显碱性 | 向三份完全相同的稀盐酸中分别加入甲、乙、丙三种金属,则甲、乙的金属活动性比丙的强 | 用等质量、等浓度的双氧水分别制取氧气 | 将a、b、c三种物质的饱和溶液分别由t1℃升温至t2℃时,所得溶液变成不饱和溶液 |
A.AB.BC.CD.D